
【题目】在“宏观一微观一符号”之间建立联系是化学学科特有的思维方式,我国科学家在水煤气变换中引入了高效催化体系,使该反应可在120℃时进行,反应过程如图所示。下列说法错误的是
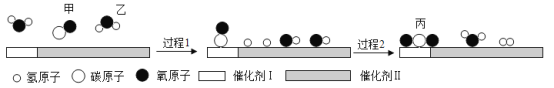
A.反应前后原子的总数不变
B.水分子是由两个氢原子和一个氧原子构成的
C.该过程体现了催化剂吸附微粒的选择性
D.反应每消耗14g甲,可生成22g丙
科目:初中化学 来源: 题型:
【题目】艾草中含有丰富的黄酮素(化学式为C15H10O2),其药用价值非常高。回答下列问题:
(1)黄酮素组成中含_____种元素,它属于_____(填“无机物”或“有机物”)。
(2)黄酮素中氢、氧元素的质量比为_____(填最简整数比)。
(3) 22.2g黄酮素中含碳元素的质量与_____g二氧化碳中所含的碳元素质量相当。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有含HCl和CuCl2的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图所示。
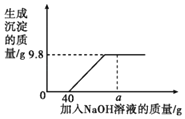
(1)恰好完全反应时,消耗NaOH溶液的总质量为_____g。
(2)求恰好完全反应时所得溶液溶质的质量分数_____(结果保留1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为某反应的微观模拟示意图。从图中获得的有关信息错误的是( )

A. 该化学反应属于分解反应
B. 原子是化学变化中的最小粒子
C. 分子之间存在一定的间隙
D. 化学反应前后原子的数目没有增减
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据所学知识并结合下图所示装置回答问题。
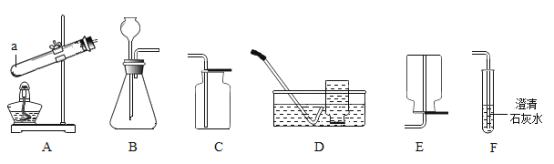
(1)用装置B制取氧气的化学方程式为________;
(2)用分解高锰酸钾的方法制取氧气,选择A做发生装置,实验中可能发生试管炸裂,将其改进的方法是________;
(3)乙炔是一种无色、 无味、难溶于水的气体,密度与空气相近。收集乙炔气体时可选择的装置是____。
(4)同学们用B、F组合,选用浓盐酸和块状石灰石反应制取二氧化碳并检验其性质,实验中始终没有发现石灰水变浑浊。小英认为所用的澄清石灰水已变质:小青认为得到的二氧化碳中混有________。为证明猜想进行了如下实验:
Ⅰ.小英将气体通入到新制的澄清石灰水中,仍未发现石灰水变浑浊
Ⅱ.小青取_______与块状石灰石反应制取CO2,并将产生的气体通入原澄清石灰水中,澄清石灰水变浑浊。分析上述实验得出的结论是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】常温下,H2O2分解生成O2的速率较为缓慢。研究性学习小组选择“H2O2分解生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
(提出假设)催化剂的种类会影响H2O2分解生成O2的快慢。
(供选择的试剂)5%H2O2溶液、15%H2O2溶液、30%H2O2溶液、二氧化锰粉末、二氧化锰颗粒、氧化铜粉末
(设计方案)常温下,取两份5%H2O2溶液各100mL,分别加入_________,测量各生成一瓶相同O2所需的时间。
(实验探究)如图是他们进行实验的装置图,此实验中A处宜采用的气体收集方法是______。检查装置气密性良好,将分液漏斗中的液体加入锥形瓶中,立即收集一瓶气体。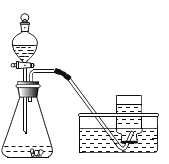
(实验记录)
实验编号 | ① | ② |
反应物 | 5%H2O2溶液100mL | 5%H2O2溶液100mL |
加入固体 | CuO | MnO2 |
收集一瓶气体所需时间 | 165s | 46s |
(实验分析)(1)若要证明二氧化锰、氧化铜是该反应的催化剂,还需要验证它们在化学反应前后的___和___没有改变。
(2)要定量地比较化学反应速度的快慢,除了上述方法外,还可以_________。
(得出结论)该探究过程得出的结论是____________,故实验室用H2O2溶液制取氧气的化学方程式为________。
(反思)还有哪些因素可能影响该反应的速率呢?
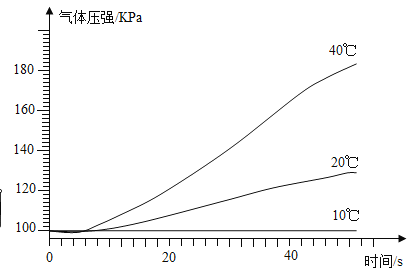
(1)在老师的帮助下,小组同学们使用压强传感器气体压强等设备,探究在其他条件相同时,不同温度下过氧化氢溶液分解时密闭容器内压强的变化。经过实验数据处理等,获得如图所示的压强-时间的曲线变化图。由此得出的结论是___________。
(2)你还有其他的猜想吗?
猜想:_____________。
请选择题目中提供的试剂,设计实验证明你的猜想(包括实验方案和结论)_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用2g石灰石样品,把20g稀盐酸(氯化氢的水溶液)分4次加入样品中(样品中除碳酸钙外,其余成分既不与盐酸反应,也不溶解于水),充分反应后经过滤、千燥等操作,最后称量,得实验数据如下:
稀盐酸的用量 | 剩余固体的质量 |
第一次加入5.0g | 1.4g |
第二次加入5.0g | 0.8g |
第三次加入5.0g | 0.2g |
第四次加入5.0g | 0.2g |
(1)从以上数据可知,这四次实验中,第________________次石灰石样品中碳酸钙已完全反应,判断的依据是__________________。
(2)求该石灰石样品与稀盐酸反应产生的二氧化碳质量。______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。

已知:Sn+SnCl4=2SnCl2
(1)SnCl4中锡元素的化合价是_____________________。
(2)铜的金属活动性比锡的________(填“强”或“弱”),固体A中一定含有的金属元素是_______。
(3)写出步骤②发生反应的化学方程式________________________________________。
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是__________________(回答一点即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】新药帕拉米韦(化学式为C15H28O4N4)注射液可用于治疗H7N9型禽流感。下列关于帕拉米韦的说法正确的是(相对原子质量:C—12、H—1、O—16、N—14)
A.帕拉米韦的相对分子质量为328 g
B.帕拉米韦是由15个碳原子、28个氢原子、4个氧原子、4个氮原子构成的
C.帕拉米韦是由碳、氢、氧、氮四种元素组成的
D.帕拉米韦中碳元素的质量分数为 ![]() ×100%
×100%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com