
 为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸.反应过程中生成的气体与所用硫酸溶液的质量关系如图所示.试计算:
为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入9.8%的稀硫酸.反应过程中生成的气体与所用硫酸溶液的质量关系如图所示.试计算:分析 根据生成的氢气的质量和对应的锌与硫酸反应的化学方程式求算锌的质量以及生成的硫酸锌的质量和参加反应的硫酸中溶质的质量,进而求算铜的质量以及消耗的硫酸溶液的质量,最后求算恰好完全反应时所得溶液中硫酸锌的质量分数.
解答 解:100ml浓硫酸(溶质质量分数为98%,密度为1.84g/ml)的质量为100mL×1.84g/mL=184g
设得到的9.8%的稀硫酸的质量为x
根据溶液稀释过程中溶质的质量不变可得
184g×98%=9.8%x
x=1840g
则加入的水的质量为1840g-184g=1656g
由图可以看出,生成的氢气的质量为0.10g
设样品中锌的质量为y,消耗的稀硫酸中溶质的质量为z,生成的硫酸锌的质量为a
Zn+H2SO4=ZnSO4+H2↑
65 98 161 2
y z a 0.10g
$\frac{65}{y}$=$\frac{98}{z}$=$\frac{161}{a}$=$\frac{2}{0.10g}$
y=3.25g
z=4.9g
a=8.05g
则铜的质量为10g-3.25g=6.75g
得到的硫酸锌溶液中硫酸锌的质量分数为$\frac{8.05g}{3.25g+4.9g÷9.8%-0.10g}$×100%≈15.1%
答:
(1)样品中铜的质量为6.75g;
(2)若将100ml浓硫酸(溶质质量分数为98%,密度为1.84g/ml)加水稀释成9.8%的稀硫酸,需加水的质量为1656g.
(3)A点时所得溶液中溶质的质量分数 15.1%
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


 全能练考卷系列答案
全能练考卷系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 归类 | 物质或现象 |
| A | 化石燃料 | 煤、石油、天然气 |
| B | 常见的碱 | 烧碱、熟石灰、纯碱 |
| C | 营养物质 | 淀粉、油脂、蛋白质 |
| D | 环境问题 | 酸雨、温室效应、PM2.5超标 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:计算题
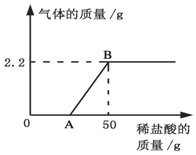 某兴趣小组在实验室发现一瓶敞口久置的氢氧化钠固体.为测定氢氧化钠的变质情况,他们取9.3g变质的氢氧化钠样品于烧杯中,加人42.9g水使其完全溶解,再向烧杯中滴加稀盐酸至过量.测得生成气体质量与所加稀盐酸质量关系如图所示.
某兴趣小组在实验室发现一瓶敞口久置的氢氧化钠固体.为测定氢氧化钠的变质情况,他们取9.3g变质的氢氧化钠样品于烧杯中,加人42.9g水使其完全溶解,再向烧杯中滴加稀盐酸至过量.测得生成气体质量与所加稀盐酸质量关系如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com