
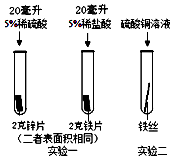
 小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图所示的两个实验:
小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图所示的两个实验:科目:初中化学 来源: 题型:填空题
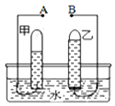 3月22日是“世界水日”,水与人类的生活和生产密切相关,请回答下列问题:
3月22日是“世界水日”,水与人类的生活和生产密切相关,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 偏大 | B. | 偏小 | C. | 不变 | D. | 无法判断 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实 验 操 作 | 实 验 现 象 | 实 验 结 论 |
| 室温下,将大小相同并打磨光亮的铬片、铝片、铜片分别投入盛有体积相同、浓度相同的稀硫酸的试管中 | 铬片表面产生气泡缓慢 铝片表面产生气泡较快 铜片表面无气泡产生 | 猜想③(填序号)成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
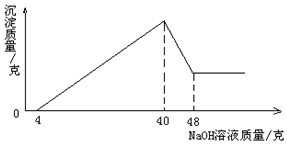 准确称取5克铝土矿(含Al2O3,Fe2O3,SiO2)样品,放入盛有50克某质量分数的硫酸溶液的烧杯中,充分反应后过滤,再向滤液中加入20%的氢氧化钠溶液,产生沉淀的质量与所加入的氢氧化钠溶液质量的关系如图所示.
准确称取5克铝土矿(含Al2O3,Fe2O3,SiO2)样品,放入盛有50克某质量分数的硫酸溶液的烧杯中,充分反应后过滤,再向滤液中加入20%的氢氧化钠溶液,产生沉淀的质量与所加入的氢氧化钠溶液质量的关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
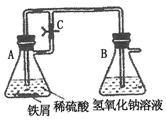 某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案:
某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案:| 资料名称 | 物理性质描述 | 化学性质描述 |
| 《化学辞典》,顾翼东编,1989年版P637 | 白色无定形粉末或白色至淡绿色六方晶体 | 与空气接触易被氧化,将细粉喷于空气中,则立即燃烧出火花 |
| 《大学普通化学(下册)》傅鹰著P637 | 白色沉淀 | 此沉淀易被氧化成微绿色Fe3(OH)8 |
| 《普通化学教程》(下册)P788 | 白色 | 能强烈吸收O2,迅速变成棕色Fe(OH)3.这时作为氧化的中间产物为土绿色,其中含有Fe2+、Fe3+. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 青蒿素的相对分子质量为282克 | |
| B. | 青蒿素中氧元素的质量分数为11.9% | |
| C. | 青蒿素中C、H、O三种元素的质量比为90:11:40 | |
| D. | 青蒿素由15个碳原子、22个氢原子和5个氧原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com