
【题目】砷化镓(![]() )是一种“LED”绿色节能光源材料,镓元素的相关信息如下所示。
)是一种“LED”绿色节能光源材料,镓元素的相关信息如下所示。
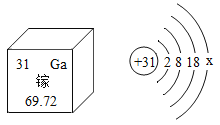
(1)镓的相对原子质量为______。
(2)在镓的原子结构示意图中![]() 的值为______。由此我们可以推断出镓元素在形成化合物时一般会显示______的化合价(填化合价的数值)。
的值为______。由此我们可以推断出镓元素在形成化合物时一般会显示______的化合价(填化合价的数值)。
(3)镓排在金属活动性顺序中氢的前面,请写出其与盐酸反应的化学方程式:________。
科目:初中化学 来源: 题型:
【题目】下列几种说法不正确的是( )
A.1个Ne原子和1个NH3分子所含质子数均为10B.S2-和S质子数相同,但化学性质不同
C.Na+、Mg2+的核外电子排布相同D.KClO3和NaClO2中氯元素的化合价相同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】初中化学教材中的一些实验如图,请你回答下列问题:
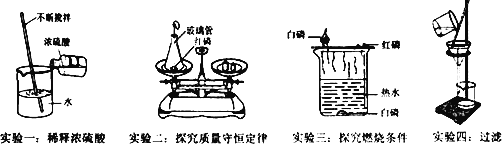
(1)实验一玻璃棒不断搅拌的目的是 _________ ;
(2)实验二锥形瓶内产生的主要现象是 _________ ;
(3)由实验三除了能得出可燃物燃烧的条件外,还可以比较出白磷、红磷化学性质上的不同点是 _________
(4)实验四得到的滤液仍然浑浊,原因是 _________ (答一点即可)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】石灰石是常见的主要矿石之一,学校研究性学习小组为了测定某矿山石灰石中碳酸钙的质量分数,取来一些矿石样品,并取来稀盐酸200g,平均分成4份,进行实验,结果如下:
实验 | 1 | 2 | 3 | 4 |
加入样品的质量(g) | 5 | 10 | 15 | 20 |
生成CO2的质量(g) | 1.76 | 3.52 | 4.4 | m |
(1)表中m的数值是______。
(2)试计算这种石灰石中碳酸钙的质量分数_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有一包混有少量Na2CO3和CaCO3的NaCl固体,为除去其中的杂质,设计流程如图,请回答下列问题:
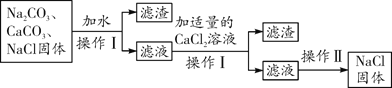
(1)在操作Ⅰ前加入水的目的____________。
(2)操作II名称是__________,其中玻璃棒的作用是__________
(3)写出除杂过程中发生的化学方程式__________。该反应属于____________(填写基本反应类型)。
(4)求出Na2CO3中碳元素的化合价:______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列知识归纳,完全正确的一组是( )
A.能量变化:①电解水是将电能转化成化学能;②煤燃烧是将化学能转化成内能;③在化学反应中只有燃烧才能放出热量。
B.环境保护:①合理施用化肥和农药;②重复使用塑料袋和塑料盒;③工业“三废”处理达标后排放。
C.数字含义:①Fe2+:一个亚铁离子带2个单位正电荷;②![]() :氧化镁中镁元素显+2价;③SO3:一个三氧化硫分子中含有3个原子。
:氧化镁中镁元素显+2价;③SO3:一个三氧化硫分子中含有3个原子。
D.资源节约:①废旧金属回收利用;②提倡使用乙醇汽油③实验后用剩药品放回原瓶
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是常见酸、碱、盐之间的相互转化关系.
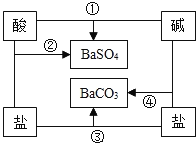
(1)写出图中相应物质的化学式:酸_____________碱____________
(2)图中反应②的化学方程式:___________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】绿矾(![]() )是硫酸法生产钛白粉的主要副产物,可用于制备
)是硫酸法生产钛白粉的主要副产物,可用于制备![]() ,复印用
,复印用![]() 粉、还原铁粉等,开发利用绿矾工艺是一项十分有意义的工作。某研究性小组展开了系列研究。
粉、还原铁粉等,开发利用绿矾工艺是一项十分有意义的工作。某研究性小组展开了系列研究。
Ⅰ制备![]()
(资料一)
①无水硫酸铜遇水变成蓝色的硫酸铜晶体。
②绿矾(![]() )高温分解产生一种金属氧化物和几种气态非金属氧化物。
)高温分解产生一种金属氧化物和几种气态非金属氧化物。
③![]() 是无色有窒息性臭味的有毒气体,能使品红溶液褪色。
是无色有窒息性臭味的有毒气体,能使品红溶液褪色。
甲同学用如下装置制备![]() 并验证绿矾受热分解的其他产物;
并验证绿矾受热分解的其他产物;
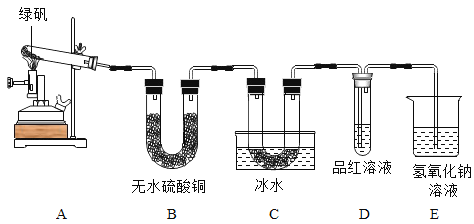
(1)实验过程中发现:A中有______色固体生成,B中无水硫酸铜变蓝,C中U形管内有无色晶体(![]() )析出,D中品红溶液褪色,装置E的作用是______,E的反应的化学方程式为______。绿矾高温分解的化学方程式为______。
)析出,D中品红溶液褪色,装置E的作用是______,E的反应的化学方程式为______。绿矾高温分解的化学方程式为______。
Ⅱ制备Fe3O4
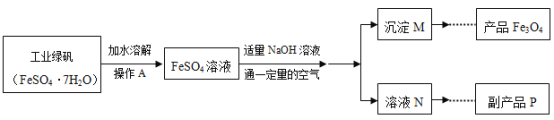
乙同学模拟生产复印用![]() 粉的实验流程如下:
粉的实验流程如下:
(资料二)①![]() 是一种白色难溶于水的固体,在空气中易被氧化成
是一种白色难溶于水的固体,在空气中易被氧化成![]() 。
。
(1)![]() 溶液中加入NaOH溶液,反应的化学方程式依次为①______,②____。由沉淀M获得
溶液中加入NaOH溶液,反应的化学方程式依次为①______,②____。由沉淀M获得![]() 的化学方程式为:
的化学方程式为:![]()
(2)控制“一定量空气”的目的是控制![]() 的转化率,沉淀M中
的转化率,沉淀M中![]() 和
和![]() 的最佳质量比为______。
的最佳质量比为______。
(3)副产品P是![]() 晶体,从溶液N获得该晶体的操作顺序是b→______→______→d
晶体,从溶液N获得该晶体的操作顺序是b→______→______→d
a过滤 b加热浓缩 c冷却结晶 d加热至完全失去结晶水
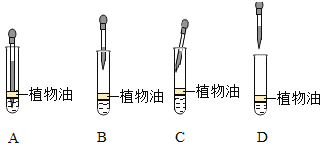
(4)若制取![]() ,采取的实验操作是:向盛有5mL新制
,采取的实验操作是:向盛有5mL新制![]() 溶液的试管中加入10滴植物油,然后用胶头滴管加煮沸的NaOH溶液(驱赶
溶液的试管中加入10滴植物油,然后用胶头滴管加煮沸的NaOH溶液(驱赶![]() ),胶头滴管的正确使用方法是______(填字母)。
),胶头滴管的正确使用方法是______(填字母)。
Ⅲ制备还原铁粉
制备还原铁粉的工业流程如下:
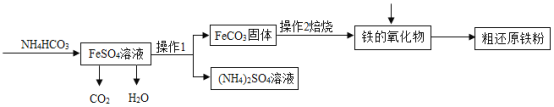
(1)操作1的名称是______, ![]() 和
和![]() 溶液反应的化学方程式为______。
溶液反应的化学方程式为______。
(2)若将14.06g粗还原铁粉(假设粗还原铁粉中杂质仅含少量![]() )在氧气流中完全反应,得到0.22g
)在氧气流中完全反应,得到0.22g![]() ,将相同质量的粗还原铁粉与足量稀硫酸反应,得到048g
,将相同质量的粗还原铁粉与足量稀硫酸反应,得到048g![]() (
(![]() 与稀硫酸不反应)。试通过计算确定
与稀硫酸不反应)。试通过计算确定![]() 的化学式(请写出计算过程)______。
的化学式(请写出计算过程)______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将一定质量的Ca(OH)2溶液与Na2CO3溶液混合恰好完全反应,向反应后的混合物中加入稀盐酸,产生气体的体积与加入稀盐酸的体积的关系如图所示,下列说法中正确的是( )
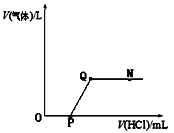
A. N 点时,所得溶液的pH=7
B. Q点时,所得溶液中的溶质只含有CaCl2
C. O至P段发生反应的化学方程式为NaOH+HCl=NaCl+H2O
D. P至Q段发生反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com