


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2013届江苏省扬州市扬中教育集团树人学校九年级中考第三次模拟考化学卷(带解析) 题型:填空题
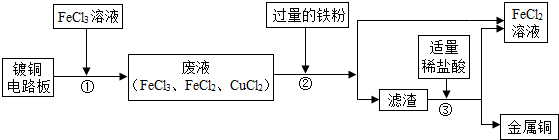
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液(主要含有FeCl2和CuCl2)处理和资源回收的工业流程如下:
试回答下列问题:
(1)过程①中Cu和FeCl3反应的化学方程式: ;过程②加入铁屑后发生的置换反应的化学方程式: ;
(2)步骤②得到滤渣的成分是 ;步骤③的操作是过滤、 、干燥等。
(3)Fe(OH)2与O2和H2O反应生成 色Fe(OH)3。写出相关的化学方程式为: 。
查看答案和解析>>
科目:初中化学 来源:2013届江苏省南通市海安县九年级学业水平测试(一模)化学试卷(带解析) 题型:填空题
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液(主要含有FeCl2和CuCl2)处理和资源回收的过程简述如下:
I:向废液中投入过量铁屑,充分反应后分离出固体和滤液;
II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
试回答下列问题:
⑴过程I加入铁屑的主要作用是 ;试写出其对应的化学方程式: ;
⑵从固体中分离出铜需采用的方法是 ;
⑶滤液中溶质主要为 (写出化学式);已知过程II生成的最终产物为Fe(OH)3,则Fe(OH)2与氧气和水反应的化学方程式为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com