
| 次数 | 1 | 2 | 3 | 4 |
| 加入盐酸质量 | 5.0g | 5.0g | 5.0g | 5.0g |
| 剩余固体的质量 | 1.5g | 1.0g | 0.5g | 0.5g |
分析 (1)根据石灰石的质量去掉杂质的质量为石灰石中碳酸钙的质量进行分析;
(2)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,依据碳酸钙的质量求出生成二氧化碳的质量.
解答 解:(1)由表中数据可知最终剩余的固体的质量0.5g就是样品中杂质的质量,所以样品中碳酸钙的质量分数为:$\frac{2g-0.5g}{2g}$×100%=75%;
(2)设产生二氧化碳的质量是x,
CaC03+2HCl=CaCl2+C02↑+H20
100 44
1.5g x
$\frac{100}{1.5g}$=$\frac{44}{x}$
x=0.66g
故答案为:(1)石灰石样品中碳酸钙的质量分数是75%;
(2)产生二氧化碳的质量是0.66g.
点评 本题主要考查有关含杂质物质的化学方程式计算,难度较大.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
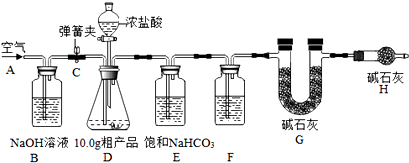
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 有发光发热的一定是燃烧 | |
| B. | 燃烧一定有火焰 | |
| C. | 燃烧一定有化学变化 | |
| D. | 要使火熄灭,必须使可燃物隔绝空气,而且使温度降到着火点以下 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
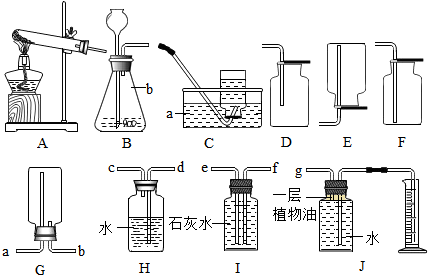
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
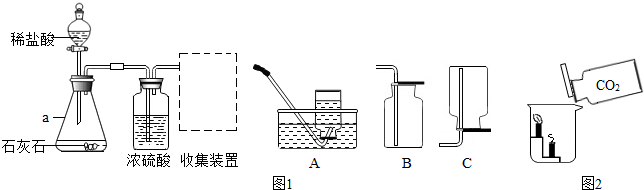
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com