
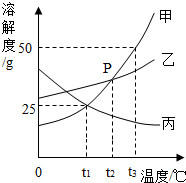
 如图是甲、乙、丙三种固体物质的溶解度曲线,请根据溶解度曲线回答下列问题:
如图是甲、乙、丙三种固体物质的溶解度曲线,请根据溶解度曲线回答下列问题:分析 (1)根据曲线中交点的含义考虑;
(2)据饱和时质量分数的计算式$\frac{溶解度}{溶解度+100g}$×100%分析解答;
(3)据甲、丙的溶解度受温度影响情况分析解答;
(4)A、根据物质溶解度的变化判断是否饱和;
B、根据t3℃时甲、丙的溶解度分析等质量的饱和溶液中溶剂质量关系,降低温度溶剂的质量不变;
C、根据甲、丙的溶解度随温度变化情况分析降温后溶液的质量变化;
D、根据饱和溶液溶质质量分数的计算,并结合二者的溶解度随温度变化分析
解答 解:(1)曲线中交点表示该温度时两种物质的溶解度相等,所以t2℃时,甲乙两种物质的溶解度相等.
(2)根据:饱和溶液的质量分数计算:$\frac{溶解度}{溶解度+100g}$×100%设溶质质量分数为200%的乙物质溶液正好饱和,则溶质的质量分数是20%,该温度下的溶解度是x,则:$\frac{x}{100g+x}$×100%=20%,解得x=25g,因为在t1℃正好是25g,所以要配制20%的乙物质溶液,必须大于t1℃才行;
(3)甲的溶解度受温度影响较大,乙的溶解度受温度影响较小,所以甲物质中混有少量的乙物质,可以采用降温结晶或冷却热饱和溶液的方法分离提纯;
(4)A、丙的溶解度随温度降低而增大,温度从t3℃降温到t1℃丙的饱和溶液会变成不饱和溶液.甲饱和乙不饱和故错误;
B、t3℃时甲的溶解度大于丙的溶解度,因此该温度下,100g甲、丙的饱和溶液中甲的饱和溶液中溶质质量大,溶剂质量就小,故溶剂甲小于丙,降温溶剂质量不变,故正确;
C、降低温度甲的溶解度减小会析出晶体而使溶液质量减小,丙的溶解度随温度降低而增大,不会结晶析出故溶液质量不变.所以甲溶液的质量小于丙溶液的质量,故错误;
D、丙的溶解度随温度降低而增大不会结晶析出,溶质质量分数不变,等于算式$\frac{溶解度}{溶解度+100g}$×100%溶解度是t3℃时乙的溶解度;甲的溶解度随温度降低而减小会析出晶体仍然饱和,饱和溶液溶质质量分数=算式$\frac{溶解度}{溶解度+100g}$×100%,溶解度是t1℃时甲的溶解度.t1℃时甲的溶解度大于t3℃时丙的溶解度,所以若分别将100g甲、丙的饱和溶液从t3℃降温到t1℃,溶质质量分数甲大.故正确;
答案:(1)t2℃时,甲乙两种物质的溶解度相等.
(2)≥t1℃;
(3)降温结晶;
(4)BD.
点评 解答本题的关键是要知道溶解度曲线表示的意义,饱和溶液中溶质质量分数的计算,溶解度大小的比较,并结合题意分析解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 地球上的陆地淡水储量约占2.53%,但是可利用的淡水资源不足0.1% | |
| B. | 使化石燃料充分燃烧,既可以减少空气污染,又可以节约化石能源 | |
| C. | 可燃冰是乙醇水合物,外观像冰,具有能量高,燃烧值大等优点 | |
| D. | 石油分解后可得到汽油、煤油、柴油等一系列产品 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe2O3发生了氧化反应,CO具有还原性 | |
| B. | 反应中铁元素的化合价升高 | |
| C. | 该反应属于分解反应 | |
| D. | 产物中有单质和氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 生铁、石油-混合物 | B. | 塑料、纤维、橡胶-合成材料 | ||
| C. | 木炭、硫酸-可燃物 | D. | 不锈钢、铜-金属材料 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 铝、铁、铜是人类广泛使用的三种金属,回答下列问题.
铝、铁、铜是人类广泛使用的三种金属,回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com