
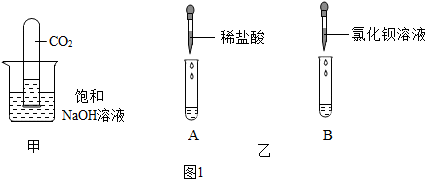
分析 (1)氢氧化钠和水都能够和二氧化碳反应,且二氧化碳也可以溶解于水,结合对出的实验现象无法准确说明液面的变化是氢氧化钠所致还是水的影响;
(2)采取的实验思路是检验对应的生成物,也就是确定是否会生成碳酸盐,用盐酸检验碳酸盐借助的是气泡生成,借助可溶性钡盐是利用的碳酸钡难溶,对应的实验现象是变浑浊或者是生成白色沉淀;
(3)物质的用途与性质密切相关,氢氧化钠溶解度大,但是和二氧化碳反应物明显现象.氢氧化钙溶解度小,但是遇到二氧化碳变浑浊;
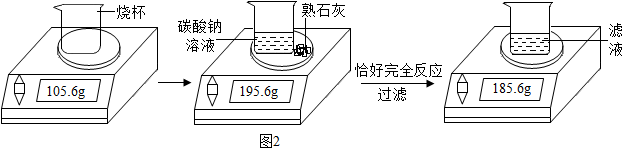
(4)根据质量守恒定律可知,过程中质量的减少是因为生成了碳酸钙,所以可以 求算碳酸钙的质量,根据碳酸钙和对应的化学方程式求算氢氧化钠的质量,进而求算对应的质量分数.
解答 解:
(1)氢氧化钠溶液中既有氢氧化钠也有水,而这两者都能和二氧化碳反应,都会引起液面上升,两者反应的化学方程式为 2NaOH+CO2=Na2CO3+H2O和H2O+CO2=H2CO3;同时二氧化碳还能溶解于水.
(2)小红设计了如下方案:分别取上述实验后的溶液于A、B两支试管中(如图乙所示),向试管A中滴加足量的稀盐酸,由于碳酸钠和盐酸反应生成二氧化碳和水以及氯化钠,对应的现象是 有气泡产生,对应的化学方程式为 Na2CO3+2HCl═2NaCl+H2O+CO2↑.向试管B中滴加氯化钡溶液,是碳酸钠和氯化钡反应生成难溶性碳酸钡和氯化钠,对应的现象是 变浑浊或者有白色沉淀产生,对应的化学方程式为 Na2CO3+BaCl2=BaCO3↓+2NaCl.
(3)氢氧化钠的溶解度远远大于氢氧化钙,所以吸收二氧化碳用氢氧化钠,而氢氧化钠和二氧化碳无明显现象,氢氧化钙和二氧化碳有明显的浑浊,所以吸收二氧化碳用氢氧化钠检验二氧化碳用氢氧化钙.吸收可以不需要现象,而检验需要明显的实验现象.
(4)根据质量守恒定律可得,生成的碳酸钙的质量为195.6g-185.6g=10g
设生成的氢氧化钠的质量为x
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
100 80
10g x
$\frac{100}{80}$=$\frac{10g}{x}$
x=8g
则所得溶液中氢氧化钠的质量分数为$\frac{8g}{185.6g-105.6g}$×100%=10%
故答案为:
(1)2NaOH+CO2=Na2CO3+H2O;二氧化碳被水溶解或者反应.
(2)有气泡产生;Na2CO3+2HCl═2NaCl+H2O+CO2↑; 变浑浊或者有白色沉淀产生; Na2CO3+BaCl2=BaCO3↓+2NaCl.
(3)氢氧化钠的溶解度远远大于氢氧化钙,所以吸收二氧化碳用氢氧化钠,而氢氧化钠和二氧化碳无明显现象,氢氧化钙和二氧化碳有明显的浑浊,所以吸收二氧化碳用氢氧化钠检验二氧化碳用氢氧化钙.
(4)10;10%
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题


查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物 质 | A | B | C | D |
| 反应前的质量/g | 18 | 18 | m | 3 |
| 反应后的质量/g | 0 | 30 | 待测 | 9 |
| A. | 该反应一定是化合反应 | |
| B. | C物质在该反应中一定是催化剂 | |
| C. | 反应后待测的C物质的质量为21g | |
| D. | 参加反应或生成的A、B、D三种物质的质量比为3:2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| Cl- | SO42- | CO 32- | NO3- | |
| H+ | 溶 | 溶 | 溶 | 溶 |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 溶 | 微溶 | 不溶 | 溶 |
| K+ | 溶 | 溶 | 溶 | 溶 |
| Mg2+ | 溶 | 溶 | 不溶 | 溶 |
| Ba2+ | 溶 | 不溶 | 不溶 | 溶 |
| A. | H2SO4 NaCl Na2CO3 CaCl2 | B. | HCl NaOH CuSO4 MgSO4 | ||
| C. | Na2CO3 K2SO4 BaCl2 HCl | D. | NaNO3 HCl CaCl2 KOH |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 活性炭作吸附剂 | B. | 稀盐酸作除锈剂 | ||
| C. | 碘酒作消毒剂 | D. | 熟石灰用于改良酸性土壤 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 自觉遵守禁鞭规定 | |
| B. | 堆放易燃物和易爆物,不能堆得过高、过密 | |
| C. | 楼内着火后,乘坐电梯快下 | |
| D. | 在火场的浓烟中逃生时,用湿毛巾捂住口鼻以减少烟气的吸入 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com