
 碘元素对青少年智力发育影响很大,我国从1994年开始强制食盐加碘量,即在食盐中加入碘酸钾(KIO3),以防止碘缺乏病的发生.由原来每千克食盐含碘40mg下调至25mg.如图是加碘食盐标签上的部分文字说明.
碘元素对青少年智力发育影响很大,我国从1994年开始强制食盐加碘量,即在食盐中加入碘酸钾(KIO3),以防止碘缺乏病的发生.由原来每千克食盐含碘40mg下调至25mg.如图是加碘食盐标签上的部分文字说明.| 相对原子质量×原子个数 |
| 相对分子质量 |
| 127 |
| 214 |


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:初中化学 来源: 题型:
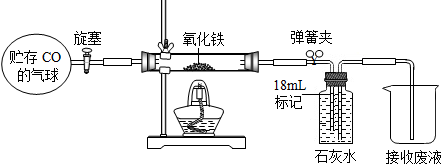
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
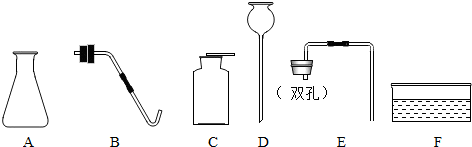
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验编号 | 实验一 | 实验二 |
| 实验装置 | 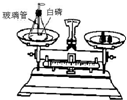 | 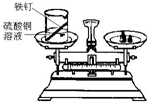 |
| 实验操作 | 将如上图所示装置放在天平上称量后取下,将玻璃管烧至红热后,迅速插入锥形瓶中,点燃白磷,并塞紧瓶塞,待反应结束,冷却后,放回托盘天平观察天平. | 将铁钉和盛有硫酸铜溶液的烧杯一起放在托盘天平上称量后取下,将铁钉浸泡在硫酸铜溶液中一段时间待反应不再继续,再放回托盘天平上,观察天平. |
| 化学方程式 | | |
| 反应前后天平是否平衡 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2用量(克) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 所用时间(秒) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
| 实验次序 | H2O2溶液溶质质量分数 | MnO2粉末用量(克) | 收集540mL气体所用时间 | 反应后液体温度(℃) |
| 1 | 1% | 0.2 | 660秒 | 24 |
| 2 | 3% | 0.2 | 220秒 | 34 |
| 3 | 5% | 0.2 | 205秒 | 39 |
| 4 | 10% | 0.2 | 80秒 | 56 |
| 5 | 15% | 0.2 | 25秒 | 65 |
| 6 | 20% | 0.2 | 9秒 | 67 |
| 7 | 25% | 0.2 | 4秒 | 69 |
| 8 | 30% | 0.2 | 3秒 | 70 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com