
���� �����ж�����̼��������������������ЧӦ��ʹȫ�������ů��ȫ���ů�����ܵ��������ı����ڻ���ʹ��ƽ����������û�����غ����У��Լ�ʹ����ɳĮ����ũҵ�����ȣ�Ϊ�˷�ֹ����ЧӦ�Ľ�һ����ǿ������Ӧ����ʹ��ú��ʯ�͡���Ȼ���Ȼ�ʯȼ�ϣ����������̫���ܡ����ܡ����ȵ������Դ������ֲ�����֣��Ͻ��ҿ��ķ�ɭ�ֵȣ�������̼����������������˹����꣬Ҳ������������ϣ�������ˮ��Ӧ����̼�ᣬ̼���������������ʣ���Ϊ̼��ܲ��ȶ������ֽ⣮�������Դ��ú��ȼ�չ����в��������Ķ�����������������Щ����������ڿ����з�Ӧ���������������ˮ�����γ����꣮
��� �⣺��1�����������ů����Ҫ�����Ƕ�����̼����Ϊ����ЧӦ�����������̼��
��2��Ҫ���ٶ�����̼���ŷţ�Ӧ����ʹ�û�ʯȼ�ϣ��������������Դ���������ʹ�û�ʯȼ�ϣ��������������Դ��
��3����ʵ������ȡ�������岢����ͨ��ˮ�У���PH��ֽ�������ȣ����PHֵԼΪ6�������ܵ������꣬��ѧ����ʽΪH2O+CO2=H2CO3�����PH��ֽ������H2O+CO2=H2CO3��
��4��������̼������������˹�����ȣ�������
��5��������һ�ѡ�˫�н������ȿ��Է�����������ᣬҲ�ܸ��������������ijЩΣ��������泥�����ʽΪNH4N03����һ�ֳ����Ļ��ʣ�������������ֲ�������������ը����ӡ����嵺�����Ŀֲ�Ϯ����ʹ�õ�ը�������������Ϊ��Ҫ�ɷ�����ģ�
�������泥�����ʽΪNH4N03����һ�ֳ����Ļ��ʣ�������������ֲ�������������ը����ӡ����嵺�����Ŀֲ�Ϯ����ʹ�õ�ը�������������Ϊ��Ҫ�ɷ�����ģ�
���� ���������ǿ����г����ֵ����ſ��㣬�˽���ֻ�������IJ����Լ���Ӧ�ķ��δ�ʩ�ǽ���������Ĺؼ���


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �в˵ĵ�����Ҫĥһĥ--Ϊ�˼�Сѹǿ | |
| B�� | ����Ʒ��ʴ--���Ļ�ѧ�����ȶ� | |
| C�� | �ҿ����������Ĺ���ʱ���ῴ����������--�����Һ�� | |
| D�� | ����ʱ����Ŷ��˼Ӵ���--�������кͷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ǿʵ��Ч�� | |
| B�� | �ṩˮ���������뻯ѧ��Ӧ | |
| C�� | ������ȵ�������ֱ���뼯��ƿ�Ӵ�����ֹ����ƿը�� | |
| D�� | ���������Ũ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 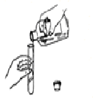 �㵹Һ�� | B�� |  ����ζ | C�� | 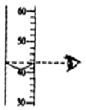 ��Һ����� | D�� | 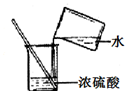 ϡ��Ũ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ȱ������ɹ������� | |
| B�� | ú��ʯ�ͺ���Ȼ���Dz��������Ļ�ʯȼ�� | |
| C�� | ����ȼ�շ�������ë�͵��� | |
| D�� | ����ɫ��Ⱦ����ָ��ɫ���ϴ���ɵ���Ⱦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
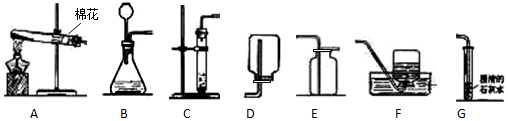
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷���ˮ����Ӳˮ����ˮ | B�� | �û���̿��ȥ���������ζ | ||
| C�� | �÷��յķ��������Ͼ����� | D�� | �����յķ���������ë�͵��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com