
| A. | 氧气 | B. | 空气 | C. | 过氧化氢 | D. | 高锰酸钾 |
科目:初中化学 来源: 题型:填空题
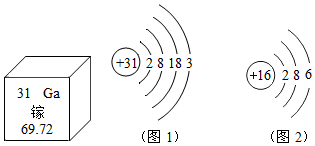 中国最年轻女院士谢毅教授因发现二维超薄半导体在提高光电、热电转换效率方面的工作,获得17届“世界杰出女科学家成就奖”.根据如图中有关镓、硫两种元素信息问答:
中国最年轻女院士谢毅教授因发现二维超薄半导体在提高光电、热电转换效率方面的工作,获得17届“世界杰出女科学家成就奖”.根据如图中有关镓、硫两种元素信息问答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | >10 mL | B. | <10 mL | C. | =10 mL | D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Mg | B. | CO2 | C. | C | D. | MgO |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 |
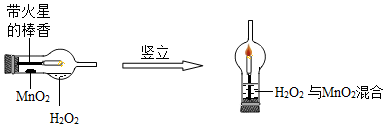
| I.分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象. | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
| II.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象. | 试管中均产生气泡,带火星木条均复燃 |
| III.将实验 II中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag. | / |
| IV.分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象. | / |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com