
黄铜是铜和锌的合金,可以用来制造机器、电器零件及日用品。为了测定某黄铜样品中铜的质量分数,取20g该样品向其中加入一定量的稀硫酸,恰好完全反应,产生氢气的质量与加入稀硫酸的质量关系如图所示。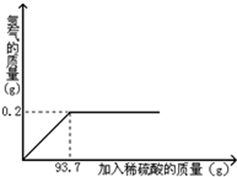
(1)完全反应后,生成H2的质量为 g。
(2)完全反应后所得溶液的溶质质量分数是多少
(保留一位小数)?
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:初中化学 来源: 题型:计算题
(3分)硫代硫酸钠(Na2S2O3)是一种用途广泛的物质。某硫代硫酸钠样品中含有少量的硫酸钠。现取16 g该样品放入烧杯中,加入113.6 g一定溶质质量分数的稀硫酸恰好完全反应,得到120 g硫酸钠不饱和溶液。
发生反应的化学方程式为:Na2S2O3 + H2SO4=== Na2SO4 + H2O + S↓+ SO2↑
请计算:
(1)样品中硫代硫酸钠(Na2S2O3)与硫酸钠的质量比。
(2)所得溶液中溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
小玉同学在实验室发现了一瓶敞口放置的过氧化氢溶液,他认为该溶液中溶质的质量分数减小了,需要重新测定并更换试剂瓶的标签。他做了如下实验:称量该溶液34.0g倒入烧杯中,然后向其中加入少量二氧化锰,直到不再放出气体后,再称量烧杯中混合物的质量,称量结果为33.7g。
(1)该溶液溶质的质量分数减小的理由是__________________________。
(2)若二氧化锰的质量是0.5g,则生成的气体的质量为___________g。
(3)计算该瓶溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某实验室用30克氯酸钾和5克二氧化锰的混合物加热制取氧气,反应一段时间后,冷却称量,得到25.4g剩余固体物质。试计算:
①生成氧气的物质的量为 摩尔。
②参加反应的氯酸钾的物质的量为 摩尔。(根据化学方程式列式计算)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
t℃时,24g镁与一定量的稀盐酸恰好完全反应,反应后得到不饱和溶液,其溶质质量分数为25%。求所用盐酸中溶质的质量分数。(答案保留0.1%,写出解题过程)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
实验室有一瓶硫酸溶液,老师请小红同学设计方案测定该废液中硫酸的质量分数。小红同学先取一洁净小烧杯,称其质量为18.2g,然后往其中倒入少量硫酸废液后称量,总质量为33.2g,之后,将一枚质量为10.8g的铁钉(已用砂纸打磨去铁锈)放入该小烧杯中反应,待铁钉表面不再有气泡产生后,再次称量,总质量为43.9 g。请回答下列问题:
(1)反应中产生的气体的质量是 。
(2)计算该废液中硫酸的质量分数(写出计算过程,计算结果保留一位小数)。
(3)若铁钉的铁锈(主要成分为氧化铁)未除净,对计算结果的影响是 (选 “偏大”、“偏小”、“无影响”),原因是 。反应方程式为
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某工厂利用废硫酸和废铁屑起反应来制取硫酸亚铁。现有废硫酸9.8 t(H2SO4的质量分数为10%)与足量的铁屑起反应,理论上可生产FeSO4的质量是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com