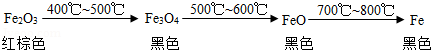铁的冶炼是钢铁工业的基础.
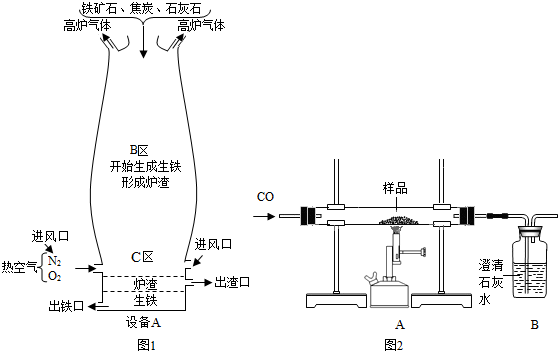
(Ⅰ)如图1是教材中炼铁高炉及炉内化学变化过程示意图,若图中采用的铁矿石的主要成分为氧化铁,请写出B区和C区所发生主要反应的化学方程式:(1)B区
(2)C区
、
.
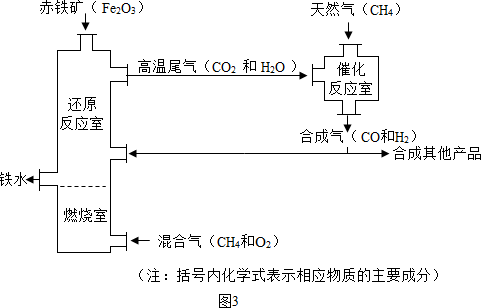
(Ⅱ)竖炉炼铁也是一种重要的炼铁方法,其工艺流程如图2所示.
(3)该工艺流程中,甲烷的作用是
燃烧产生热量
燃烧产生热量
、
做生产合成气的原料
做生产合成气的原料
,冶炼出的铁水属于
混合物
混合物
(填“纯净物”或“混合物”).
(4)该工艺流程中,可循环利用的物质是
CO2和H2O(高温尾气)
CO2和H2O(高温尾气)
.
(Ⅲ)金属在活动性顺序里的位置越后,其化合物越不稳定,所以它的氧化物越容易被还原.
(5)请在下列①②中各写一个化学方程式,③中写出还原金属氧化物的方法.

(Ⅳ)某兴趣小组同学利用图3装置进行相关实验,测定样品的组成:
(6)若样品由氧化铁、氧化亚铁和四氧化三铁中的一种或几种组成,待充分反应后,实验数据记录如下:
| 样品质量 |
装置A中玻璃管和固体的总质量 |
装置B的质量 |
| 2.32g |
反应前55.72g |
反应前 281.00g |
| 反应后55.08g |
反应后 281.56g |
请回答下列问题:
①兴趣小组同学经过讨论后认为应选用样品质量和装置A中玻璃管和固体的总质量的变化来计算,而不选用装置B的质量的变化来计算,理由是
装置B不能将反应产生的CO2全部吸收
装置B不能将反应产生的CO2全部吸收
.
②该样品所有可能的组成是
Fe3O4;Fe2O3、FeO;Fe3O4、Fe2O3、FeO
Fe3O4;Fe2O3、FeO;Fe3O4、Fe2O3、FeO
.

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案