
 构建知识网络是一种重要的学习方法.如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物.则A、B、C可能是( )
构建知识网络是一种重要的学习方法.如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物.则A、B、C可能是( )| A. | KOH、CuSO4、Na2CO3 | B. | Ba(OH)2、CuSO4、CuO | ||
| C. | Ca(OH)2、HNO3、K2CO3 | D. | NaOH、HCl、Ba(NO3)2 |
分析 由酸的通性可知:酸能跟活泼金属、金属氧化物、盐、碱等物质反应.B是由硫酸与其它物质反应制取的,且能与A、C反应,A、B、C分别属于不同类别的化合物,据此可采取带入验证的方法进行分析解答.
解答 解:由酸的通性可知:酸能跟活泼金属、金属氧化物、盐、碱等物质反应.由硫酸化学性质的知识网络图可知,B是由硫酸与其它物质反应制取的,且能与A、C反应,A、B、C分别属于不同类别的化合物.
A、CuSO4、Na2CO3均属于盐,故选项不符合要求.
B、Ba(OH)2能与稀硫酸发生中和反应,能与CuSO4反应生成氢氧化铜沉淀和硫酸钡沉淀;但CuSO4不能与CuO发生化学反应,故选项不符合要求.
C、Ca(OH)2能与稀硫酸、稀硝酸发生中和反应,且硝酸能与K2CO3反应硝酸钾、水和二氧化碳,且Ca(OH)2、HNO3、K2CO3分别属于碱、酸、盐,故选项符合要求.
D、NaOH能与稀硫酸、稀盐酸发生中和反应,但Ba(NO3)2不能与HCl发生化学反应,故选项不符合要求.
故选C.
点评 本题有一定难度,熟练掌握酸的化学性质、酸碱盐与氧化物的判别是正确解答本题的关键,采用带入验证法是正确快速、解答本题的捷径.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:初中化学 来源: 题型:实验探究题
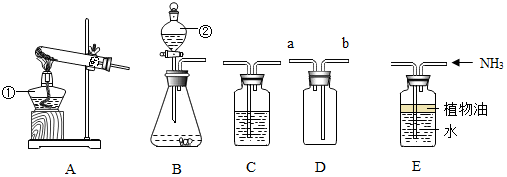
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
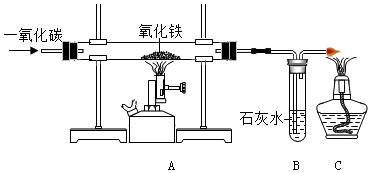
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
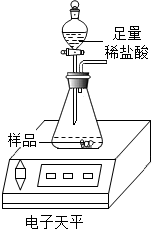 超市卖的纯碱产品中往往会含有少量的氯化钠,化学兴趣小组的同学要通过实验来测定某品牌的纯碱样品中的Na2CO3的质量分数.他们取了纯碱样品11.0g,利用如图装置进行实验测定.数据记录如表:
超市卖的纯碱产品中往往会含有少量的氯化钠,化学兴趣小组的同学要通过实验来测定某品牌的纯碱样品中的Na2CO3的质量分数.他们取了纯碱样品11.0g,利用如图装置进行实验测定.数据记录如表:| 称量项目 | 称量时间 | 质量/g |
| 样品 | 11.0 | |
| 装置+稀盐酸 | 160.0 | |
| 装置+稀盐酸+样品 | 反应开始后20s | 167.0 |
| 装置+稀盐酸+样品 | 反应开始后30s | 166.6 |
| 装置+稀盐酸+样品 | 反应开始后90s | 166.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
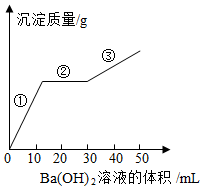 某溶液是由硫酸钠、碳酸钠、盐酸、氯化铜、硝酸钠中的一种或几种组成的.为确定其成分,向该溶液中逐渐加入氢氧化钡溶液,产生沉淀质量与加入氢氧化钡溶液体积的关系如图所示.
某溶液是由硫酸钠、碳酸钠、盐酸、氯化铜、硝酸钠中的一种或几种组成的.为确定其成分,向该溶液中逐渐加入氢氧化钡溶液,产生沉淀质量与加入氢氧化钡溶液体积的关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水烧开后易把壶盖冲起--温度升高,分子变大 | |
| B. | 氢气和液氢都可作燃料--相同物质的分子,其化学性质相同 | |
| C. | 用警犬搜救地震中被埋人员--分子在不断运动 | |
| D. | 用水银温度计测量体温--温度升高,原子的间隔变大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com