

分析 根据已有的物理变化和化学变化的区别、电解水生成氢气和氧气、铁在与水和氧气并存时易生锈等进行分析解答.
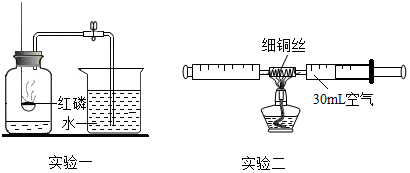
解答 解:①实验2为电解水的实验,则可书写其化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;根据质量守恒定律,得出实验结论为:由此实验得出水是由氢元素和氧元素组成的;加热水沸腾的过程中没有新物质生成,属于物理变化,水分子不变;电解水属于化学变化,水分子发生了改变,故填:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;氢、氧元素;水分子是否改变;
②A中铁丝不与水是接触,B中铁丝与水接触,说明铁生锈需要有水;B中通入的是氧气,而D中与空气接触,空气中氧气的浓度低于通入的氧气的浓度,说明铁生锈与氧气的浓度有关,故填:氧气、水;水;氧气的浓度.
点评 本题考查的是物质的变化以及铁的锈蚀条件的探究,完成此题,可以依据已有的知识进行.


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | ①②⑤⑥ | B. | ②③④⑤ | C. | ②④⑤⑥ | D. | ②⑤⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 现象 | 结论 |
| 如果装置B澄清石灰水变浑浊,装置C无现象 | 则猜想①成立 |
| 如果装置B无现象,装置C试纸由黄色变为蓝色 | 则猜想②成立 |
| 如果装置B澄清石灰水变浑浊,装置C试纸由黄色变为蓝色 | 则猜想③成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
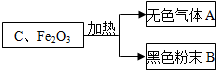
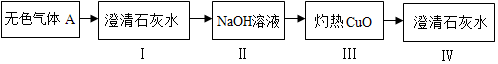
| 物质 性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
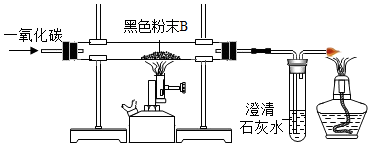
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 由一个质子和一个电子构成的 | |
| B. | 由一个带负电的质子和一个带正电的电子构成的 | |
| C. | 由一个质子和一个带正电的电子构成的 | |
| D. | 由一个带负电的质子和一个电子构成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 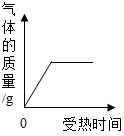 用一定质量的高锰酸钾加热制氧气 | |
| B. | 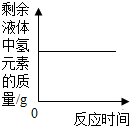 过氧化氢溶液与二氧化锰混合物制取氧气 | |
| C. | 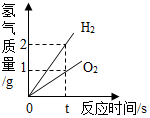 电解水实验 | |
| D. | 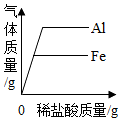 分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com