
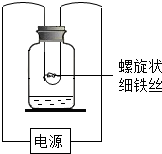
 如图所示,将细铁丝分别放在充满氮气、氧气的集气瓶中进行实验.
如图所示,将细铁丝分别放在充满氮气、氧气的集气瓶中进行实验.| 实验 | Ⅰ | Ⅱ |
| 集气瓶中的气体 | 氮气 | 氧气 |
| 接通电源加热后观察到的现象 | 铁丝红热,不燃烧 | 剧烈燃烧,火星四射 |
分析 根据燃烧的条件、铁在氧气中燃烧的现象、注意事项及发生的反应分析回答有关的问题
解答 解:(1)实验Ⅱ中,铁丝在氧气中燃烧生成黑色固体,为防止生成物炸裂集气瓶,需集气瓶中放水;
实验一:取一根细铁丝在酒精灯火焰上灼烧,观察到的现象是红热,将其迅速插入充满氧气的集气瓶中,细铁丝未燃烧,从燃烧的条件分析原因温度未达到着火点.
(2)接通电源后,实验Ⅰ中铁丝红热,不燃烧;实验Ⅱ中剧烈燃烧,火星四射;可知可燃物燃烧的条件之一是与氧气接触;
实验现象,可知可燃物燃烧的条件之一是
(3)实验Ⅱ(或在氧气中)中,加热前不燃烧,接通电源(或加热)后燃烧,证明可燃物燃烧需要温度达到着火点.
故答为:(1)黑; 防止集气瓶底炸裂;(2)与氧气接触;
(3)实验Ⅱ(或在氧气中)中,加热前不燃烧,接通电源(或加热)后燃烧.
点评 本题难度不大,掌握常铁丝在氧气中燃烧的现象即可正确解答;在描述燃烧的现象时,需要注意光和火焰、烟和雾的区别.


 目标测试系列答案
目标测试系列答案科目:初中化学 来源: 题型:填空题
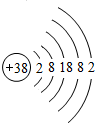 据《自然》杂志报道,科学家最近研制出一种以元素锶( Sr)的原子作钟摆的钟是世界上最精确的钟.锶原子结构示意图为:
据《自然》杂志报道,科学家最近研制出一种以元素锶( Sr)的原子作钟摆的钟是世界上最精确的钟.锶原子结构示意图为: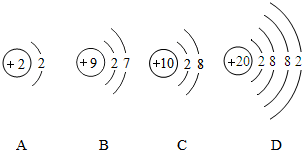
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | “超纯水”绝对卫生,长期饮用对健康有益 | |
| B. | 该饮料经过28次过滤,不含任何杂质 | |
| C. | 本饮料由天然物质配制,绝对不含化学物质 | |
| D. | 矿泉水中含钾、钙、镁等多种元素,是一种健康饮品 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
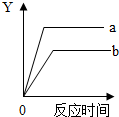 如表中所描述的变化与右图相符合的是( )
如表中所描述的变化与右图相符合的是( )| 化学变化 | Y轴 | a | b | |
| A | 等质量的高锰酸钾和水在不同条件下分解 | 氧气质量 | 高锰酸钾 | 水 |
| B | 等质量、等浓度的双氧水在不同条件下反应 | 氧气质量 | 加催化剂 | 加热 |
| C | 等质量的镁片和铁片分别与足量的稀硫酸反应 | 氢气质量 | 镁 | 铁 |
| D | 等质量的二氧化碳和生石灰分别与等量的水反应 | 温度 | 二氧化碳 | 生石灰 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 清洁剂 |  洁厕灵 |  彩漂液 |  漂白水 |
| 功 能 | 清除污垢,除异味 | 漂洗衣物,使色彩鲜艳 | 漂除衣物污渍 |
| 有效成分 | 盐酸(HCl) | 过氧化氢 | 次氯酸钠(NaClO) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 出发前购买食品.
出发前购买食品.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体剩余物于试管中,向其中加入足量的稀盐酸. | (1)固体部分溶解,溶液为无色. | 假设①成立. |
| (2)固体部分溶解,有气体生成,溶液为无色. | 假设②成立. | |
| (3)固体部分溶解,溶液为蓝色. | 假设③成立. |
| 实验组别 | I | II | III | IV | V |
| 药 品 | Al | Fe | Ag | Al | Cu |
| CuO | CuO | CuO | Fe2O3 | Fe2O3 | |
| 相同条件下是否反应 | 是 | 是 | 否 | 是 | 否 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com