
| A. | 冰川融化 | B. | 铁钉生锈 | C. | 蜡烛燃烧 | D. | 食物变质 |
分析 化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化与物理变化的本质区别是有无新物质生成,据此抓住化学变化和物理变化的区别结合事实进行分析判断即可.
解答 解:A、冰川融化的过程中只是状态发生改变,没有新物质生成,属于物理变化.
B、铁钉生锈的过程中有新物质铁锈生成,属于化学变化.
C、蜡烛燃烧的过程中有新物质二氧化碳和水等生成,属于化学变化.
D、食物变质的过程中有对人体有害的新物质生成,属于化学变化.
故选:A.
点评 本题难度不大,解答时要分析变化过程中是否有新物质生成,这里的新物质是指和变化前的物质是不同种的物质,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.


科目:初中化学 来源: 题型:解答题
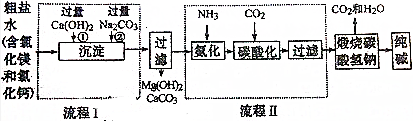
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
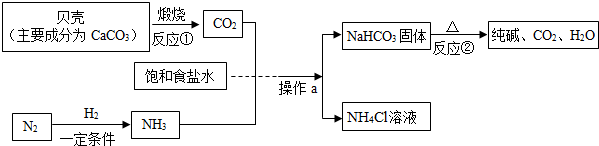
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 汽车轴承和骨架是由合金制成,轮胎是由合成橡胶制成 | |
| B. | 汽车改用压缩天然气或液化石油气做燃料,可以减少对空气的污染 | |
| C. | 少开私家车,多乘坐公共交通工具,符合“节能减碳”的环保理念 | |
| D. | 在加油站附近能闻到汽油的气味,是因为分子间存在一定的距离 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
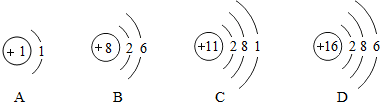
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加入明矾使小颗粒凝聚 | B. | 通入氯气杀菌消毒 | ||
| C. | 通过沙滤装置除去可溶性杂质 | D. | 通过活性炭吸附部分有害物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 是一种有机物 | B. | 由碳、氢、氧元素组成 | ||
| C. | 碳、氢、氧元素的质量比是1:2:1 | D. | 相对分子质量为30 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
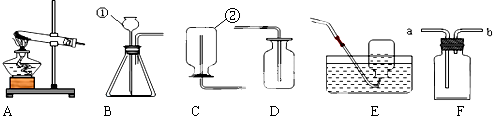
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 1926年,我国著名化学家侯德榜先生创立了侯氏制碱法,促进了我国民族工业的发展和世界制碱技术的进步,其生产过程中有下列反应:
1926年,我国著名化学家侯德榜先生创立了侯氏制碱法,促进了我国民族工业的发展和世界制碱技术的进步,其生产过程中有下列反应:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com