
【题目】我国钢铁产量居世界第一,为国民经济的发展奠定了坚实的基础,生产生活中铁和铁的化合物也有着广泛的应用。
(一)铁的广泛应用
(1)“加铁酱油”中的铁指的是_____(填“单质”或“元素”)。
(2)铁制炊具加热食物,说明铁具有的性质是_____。
(3)铁与铬、镍等金属熔合可形成“不锈钢”,用不锈钢丝和聚乙烯纤维为原料可制作耐酸防护服材料。以上叙述中没有涉及到_____(填字母)。
A 合金 B 无机非金属材料 C 合成材料 D 复合材料
(二)铁锈成分的探究
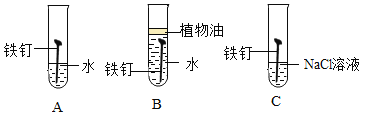
(1)下图为某兴趣小组探究铁生锈的三个实验,最先观察到铁锈的是_____(选填序号)。
(2)铁生锈的主要过程为:Fe![]() Fe(OH)2
Fe(OH)2![]() Fe(OH)3
Fe(OH)3![]() Fe2O3xH2O
Fe2O3xH2O
次要过程为:Fe![]() FeCO3
FeCO3
写出Fe→Fe(OH)2反应的化学方程式_____。
(3)铁锈组分的确定
某铁锈成分为Fe2O3xH2O和FeCO3.为确定其组成,兴趣小组称取此铁锈样品25.4g,在科研人员的指导下用下图装置进行实验。

(查阅资料)①Fe2O3xH2O失去结晶水温度为110℃,FeCO3在282℃分解为FeO和CO2
②温度高于500℃时铁的氧化物才能被CO还原。
(1)装配好实验装置后,首先要_____。
(2)装置A中的反应为:H2C2O4(草酸)![]() CO↑+CO2↑+H2O通过B、C装置可得到干燥、纯净的CO气体,洗气瓶B中应盛放_____(选填序号)。
CO↑+CO2↑+H2O通过B、C装置可得到干燥、纯净的CO气体,洗气瓶B中应盛放_____(选填序号)。
a.浓硫酸 b.氢氧化钠溶液
(3)现控制D装置中的温度为300℃对铁锈进行热分解,直至D装置中剩余固体质量不再变化为止,冷却后装置E增重3.6g,装置F增重2.2g。则样品中FeCO3的质量m(FeCO3)=_____g。
(4)若缺少G装置,Fe2O3xH2O中x的值会_____。(选填“偏大”、“偏小”、“不变”)
(三)炼铁过程的探究
(1)进行上述实验时,应先点燃A装置中的酒精灯,后对D玻璃管加热,原因是_____。
(2)将上述300℃完全分解后的D装置中剩余固体继续升温,当温度高于500℃时,铁的氧化物全部被CO还原得到铁的质量_____克。(计算过程)
【答案】元素 导热性 B C 2Fe+O2+2H2O=2Fe(OH)2 检查装置气密性 b 5.8 偏大 排出装置中的空气,防止发生爆炸 14
【解析】
解:(一)铁的广泛应用
1、“加铁酱油”中的铁指的是元素。
故填:元素。
2、铁制炊具加热食物,说明铁具有的性质是导热性。
故填:导热性。
3、铁与铬、镍等金属熔合可形成“不锈钢”,不锈钢属于合金,聚乙烯纤维属于合成材料,用不锈钢丝和聚乙烯纤维为原料可制作耐酸防护服材料属于复合材料。
故填:B。
(二)铁锈成分的探究
1、B中铁钉与氧气隔绝,不容易生锈,A中铁钉和水、氧气接触,容易生锈,C中铁钉与水和氧气接触,容易生锈,同时氯化钠溶液能够促进铁钉生锈,因此最先观察到铁锈的是C。
故填:C。
2、铁和水、氧气反应生成氢氧化亚铁的化学方程式为:2Fe+O2+2H2O=2Fe(OH)2。
故填:2Fe+O2+2H2O=2Fe(OH)2。
3、(1)装配好实验装置后,首先要检查装置气密性。
故填:检查装置气密性。
(2)洗气瓶B中应盛放氢氧化钠溶液,用来吸收二氧化碳。
故填:b。
(3)设碳酸亚铁质量为x,
装置F增重2.2g,说明碳酸亚铁分解生成了2.2g二氧化碳,
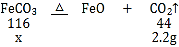
![]() =
=![]() ,
,
x=5.8g,
故填:5.8。
(4)若缺少G装置,空气中的水蒸气和二氧化碳会进入F装置,导致计算的碳酸亚铁质量偏大,从而导致Fe2O3xH2O质量偏小,而通过E装置测定的结晶水质量不变,从而导致Fe2O3xH2O中x的值会偏大。
故填:偏大。
(三)炼铁过程的探究
1、进行上述实验时,应先点燃A装置中的酒精灯,后对D玻璃管加热,原因是排出装置中的空气,防止发生爆炸。
故填:排出装置中的空气,防止发生爆炸。
2、Fe2O3的质量为:25.4g﹣3.6g﹣5.8g=16g,
16g氧化铁中铁元素质量为:16g×![]() =11.2g,
=11.2g,
5.8g碳酸亚铁中铁元素质量为:5.8g×![]() =2.8g,
=2.8g,
将上述300℃完全分解后的D装置中剩余固体继续升温,当温度高于500℃时,铁的氧化物全部被CO还原得到铁的质量为:11.2g+2.8g=14g,
故填:14。


科目:初中化学 来源: 题型:
【题目】现有如图甲所示仪器和装置,请回答下列问题:
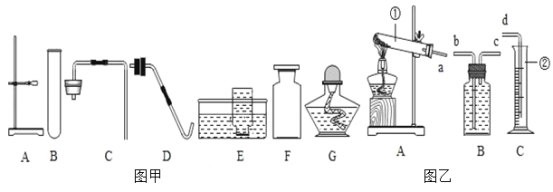
(1)写出A、G两种仪器的名称:A:_____;G:_____。
(2)用加热氯酸钾和二氧化锰的方法制取一瓶较为纯净的氧气,应从图甲中选用的仪器装置是_____(填字母编号),该实验的主要步骤有:①装药品;②检查装置的气密性;③加热;④将装置固定在铁架台上;⑤熄灭酒精灯;⑥收集气体;⑦将导管移出水槽。正确的操作顺序为_____,反应的文字表达式为_____,其中二氧化锰起_____作用。
(3)某校化学兴趣小组的同学利用如图乙所示装置进行实验。
(实验目的)粗略测定加热2g高锰酸钾所收集到的氧气体积。
(反应原理)高锰酸钾制取氧气的文字表达式为_____。
(装置连接)为达到实验目的,各装置的正确连接顺序是:a→_____(填接口的字母)→d。
(补充实验)在收集到的氧气中做细铁丝燃烧的实验:
①集气瓶内为什么要预先装少量水或铺一层细砂?_____;
②实验过程中发现B瓶中的水变红了,原因是_____入B中。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在实验室常用以下装置制取气体。

(1)选择装置A用高锰酸钾制取氧气的化学方程式为①_____,试管口放一团棉花的作用是②_____,选择此发生装置的依据③_____。
(2)用装置B制取二氧化碳的化学方程式为①_____,收集气体采用的是②_____法,实验过程中,长颈漏斗末端应位于液面下的目的是③_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用l50g溶质质量分数为98%的浓硫酸配制30%的稀硫酸的过程中,下列做法正确的是( )
A. 将l50g的浓硫酸加入490g的水中
B. 配制好的稀硫酸存放在铁制器皿中
C. 配制时把水沿容器内壁缓慢注入浓硫酸中
D. 配制稀硫酸的步骤是计算、量取、溶解、装瓶贴标签
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组的同学按图示装置及步骤验证氢氧化钠的化学性质。
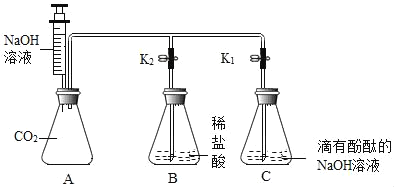
(实验步骤)
Ⅰ.将注射器内的液体注入A中的锥形瓶。
Ⅱ.打开K1,观察到C中部分红色溶液沿导管倒溶液吸入A,片刻后回流停止。
Ⅲ.打开K2,观察到B中溶液倒吸入A、C中,液面稳定后观察到A中溶液仍为红色,C中溶液变为无色。
同学们对相关问题分组展开如下探究。
探究环节 | 甲组的探究 | 乙组的探究 |
(提出问题) | A中使酚酞变为红色的物质是什么? | C中溶液为什么变成无色? |
(做出猜想) | 猜想一:Na2CO3 猜想二:Na2CO3和NaOH | 猜想一:实验过程中酚酞变质了 猜想二:溶液中的NaOH反应完了 |
(实验验证) | 小鹏取少量A中溶液于试管中,向其中滴加过量BaCl2溶液,若观察到_____,证明猜想二成立。小丽认为用Ba(OH)2溶液也可证明猜想二成立,小鹏认为小丽的方案不合理,理由是_____。 | (1)取少量C中溶液于试管中,向其中滴加NaOH溶液,溶液又变为红色,证明猜想一不成立。 (2)用pH试纸测定C中溶液的酸碱度,若pH_____,证明猜想二成立。 |
(反思交流)(1)甲、乙两组同学的实验证明了NaOH能与稀盐酸、CO2发生反应;A中溶液里一定还存在NaCl.写出NaOH与CO2发生反应的化学方程式_____。
(2)(实验步骤)Ⅱ中的现象_____(填“能”或“不能”)证明NaOH与CO2发生了反应。
(拓展迁移)对于无明显现象的化学反应,可通过检验有新物质生成或检验_____的方法来证明反应发生了。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为实验室用等质量的高锰酸钾和氯酸钾(另加少量的二氧化锰),分别制取氧气的数据分析示意图。下列依据图示信息所得出的分析正确的是( )

A. 同时开始加热,先收集到氧气的是氯酸钾
B. 用等质量的高锰酸钾和氯酸钾制取较多量的氧气时,宜选择氯酸钾
C. 加入少量的二氧化锰使氯酸钾产生的氧气质量增加
D. 反应时间较长的是高锰酸钾
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)自来水厂净水流程分:取、加、沉、滤、吸和投。“取”为从水库中取水。
①“加”为向水中加入主要成分为______(填“蓝矾”、“胆矾”或“明矾”)的絮凝剂,作用是______ 。 “沉”为在反应池中沉降分离。
②“滤”为过滤掉水中不溶性固体杂质,过滤操作中玻璃棒的作用是________。
③“吸”为将过滤所得的滤液引入吸附池,加入_________,作用是______________。
④“投”为投药消毒,发生的是___________(填“物理”或“化学”)变化。
(2)黄铜是铜和锌的合金。某化学兴趣小组为测定黄铜中铜的含量,取黄铜样品40g,放入烧杯中,向其中加入200g稀盐酸,恰好完全反应,反应后烧杯中剩余物的总质量为239.6g。求黄铜中铜的质量分数________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示为实验室中常见的气体制备和收集装置。
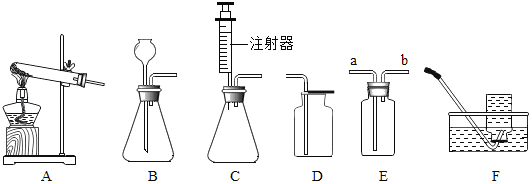
请回答下列问题:
(1)实验室用高锰酸钾制取氧气,应选用发生装置_____(填字母序号),实验时该装置试管口应放一团棉花,其目的是_____,反应的化学方程式为_____。若用装置D收集氧气,验满的方法是_____。
(2)实验室用大理石和稀盐酸制取二氧化碳,若选用C做发生装置,你认为选用C的优点是_____,反应的化学方程式为_____。
(3)欲使用装置E用排空气法收集氧气,则气体应从_____(填“a”或“b”)端通入;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从_____(填“a”或“b”)端通入。
(4)选用F装置收集气体时,下列实验操作不正确的是_____(填序号)。
a 加热前,将集气瓶装满水,用玻璃片盖住瓶口,倒立在盛水的水槽中
b 加热后,观察到水中导管口开始有气泡时,立即收集气体
c 待气泡从集气瓶口逸出时,在水面下用玻璃片盖住瓶口,移出水槽正放在桌面上
(5)已知甲烷(CH4)是一种无色无味、密度比空气小、难溶于水的气体,实验室常用加热无水醋酸钠与碱石灰的混合物来制取,则实验室制取并收集甲烷应选择的装置组合为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com