
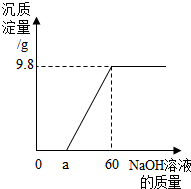
 小明在做铁置换硫酸铜的实验时,发现铁钉表面有气泡产生,经测定,知是硫酸铜中混入了少量稀硫酸,为测定溶液的组成情况,取100克混合溶液,向其中加入质量分数为20%的NaOH溶液,产生的沉淀与所加入NaOH溶液的质量关系如图:
小明在做铁置换硫酸铜的实验时,发现铁钉表面有气泡产生,经测定,知是硫酸铜中混入了少量稀硫酸,为测定溶液的组成情况,取100克混合溶液,向其中加入质量分数为20%的NaOH溶液,产生的沉淀与所加入NaOH溶液的质量关系如图:| 80 |
| 20%×x |
| 98 |
| 9.8g |
| 80 |
| 20g×20% |
| 98 |
| y |
| 4.9g |
| 100g |


科目:初中化学 来源: 题型:
| 实验操作 | ① | ② | ③ | ④ |
| 实验现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
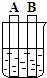
 (2008?海淀区一模)小东和小明收集了两个形状、大小、轻重和硬度均不同的易拉罐,如图所示.他们很想知道每个易拉罐的材料成分,于是展开了以下探究过程.
(2008?海淀区一模)小东和小明收集了两个形状、大小、轻重和硬度均不同的易拉罐,如图所示.他们很想知道每个易拉罐的材料成分,于是展开了以下探究过程.| 物理性质 | 银 | 铜 | 铁 | 铝 |
| 密度/(g?cm-3) | 10.5 | 8.92 | 7.86 | 2.70 |
| 硬度(以金刚石的硬度为10作标准) | 2.5~4 | 2.5~3 | 4~5 | 2~2.9 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
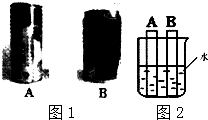 小东和小明收集了两个形状、大小、轻重和硬度均不同的易拉罐,如图1所示.他们很想知道每个易拉罐的材料成分,于是展开了以下探究过程.
小东和小明收集了两个形状、大小、轻重和硬度均不同的易拉罐,如图1所示.他们很想知道每个易拉罐的材料成分,于是展开了以下探究过程.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
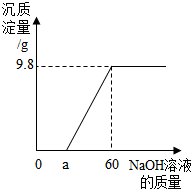 小明在做铁置换硫酸铜的实验时,发现铁钉表面有气泡产生,经测定,知是硫酸铜中混入了少量稀硫酸,为测定溶液的组成情况,取100克混合溶液,向其中加入质量分数为20%的NaOH溶液,产生的沉淀与所加入NaOH溶液的质量关系如图:
小明在做铁置换硫酸铜的实验时,发现铁钉表面有气泡产生,经测定,知是硫酸铜中混入了少量稀硫酸,为测定溶液的组成情况,取100克混合溶液,向其中加入质量分数为20%的NaOH溶液,产生的沉淀与所加入NaOH溶液的质量关系如图:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com