
科目:初中化学 来源:2020年5月江苏省常州市2020届中考模拟化学试卷 题型:简答题
2011年11月9日是全国第21个消防宣传日,今年的主题是“全民消防、生命至上”。家庭防火是其中的一个重要组成部分。
(1)下列家庭中的物品属于可燃物的有______。
a.玻璃 b.食用油 c.高度白酒 d.毛衣
(2)如图所示的“火立熄”是一种新型的家用灭火用品。“火立熄”接触到火焰3—5秒后炸开,释放的粉末覆盖在燃烧物上,同时放出不可燃气体,使火焰熄灭。“火立熄”的灭火原理是______。

(3)①工业上常利用水煤气(CO和H2)来生产甲烷,同时生成水,其化学方程式是_____。
②在使用天然气之前,很多家庭使用管道煤气(主要成份是CO),请写出天然气代替管道煤气作为家庭燃料的优点_____________。
查看答案和解析>>
科目:初中化学 来源:2020年山东省枣庄市中考二模化学试卷 题型:单选题
预防非典型肺炎要经常杀菌消毒。过氧乙酸(化学学式为CH3COOOH)是一种广谱、高效杀菌消毒剂,对预防非典型肺炎有很好作用。下列说法不正确的是
A.过氧乙酸分子是由碳、氢、氧三种原子构成
B.过氧乙酸的相对分子质量为76
C.过氧乙酸中碳、氢、氧元素的质量比是6:1:12
D.过氧乙酸是由2个碳元素,4个氢元素和3个氧元素组成的
查看答案和解析>>
科目:初中化学 来源:2017年广东省东莞市中考化学试卷 题型:单选题
镁带在耐高温的容器中(内含氧气)密封加热,下图能正确表示容器里所盛的物质总质量变化的是( )
A.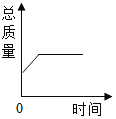 B.
B.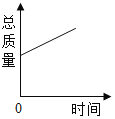 C.
C.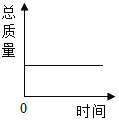 D.
D.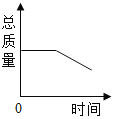
查看答案和解析>>
科目:初中化学 来源:2020年天津市河北区中考一模化学试卷 题型:填空题
根据所学化学知识回答问题。
(1)在粗盐提纯的实验中其主要的操作步骤顺序是__(填数字序号)。
①过滤
②溶解
③蒸发
④计算产率
(2)在蒸发加热过程中,应用玻璃棒不断搅拌,防止因局部温度过高,造成___;当蒸发皿中出现_时,应停止加热。
(3)欲除去粗盐中可溶性杂质Na2SO4、MgCl2、 CaCl2 得到纯净的NaCl,所加试剂为稍过量的BaCl2溶液、稍过量的___ (填化学式) 溶液、稍过量的Na2CO3溶液和适量的稀盐酸。
(4)纯净的氯化钠是重要的化工产品,熔融态的氯化钠通电可生成金属钠和氯气,写出该反应的化学方程式__。
查看答案和解析>>
科目:初中化学 来源:2020年天津市河北区中考一模化学试卷 题型:填空题
现有①维生素A②浓硫酸③甲烷④金刚石⑤二氧化氮⑥氯化钠,选择适当的物质填空(填序号)。
(1)可用来裁玻璃的是________________________。
(2)可用作干燥剂的是_______________________。
(3)可治疗夜盲症的是_______________________。
(4)可用作气体燃料的是_______________________。
(5)可造成酸雨的气体是_______________________。
(6)可用作厨房调味品的是_______________________。
查看答案和解析>>
科目:初中化学 来源:2020年北京市房山区中考一模化学试卷 题型:实验题
请从A~D中任选三个作答,若均作答,按前三个计分。如图,在Y形管中进行实验。补全实验方案。
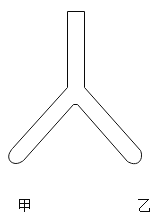
序号 | 目的 | 操作 | 现象 | 结论 |
A | 探究金属活动性 | 甲:放入铁片; 乙:放入银片; 向甲、乙处加入________ | 甲中有红色固体生成,溶液变为浅绿色; 乙中无明显变化 | 金属活动性:铁>铜> 银 |
B | 验证可燃物的燃烧条件 | 甲:放入红磷; 乙:放入白磷; 将甲、乙底部浸入80°C热水中 | 甲中无明显变化; 乙中白磷燃烧 | ________ |
C | 探究CO2的性质 | 甲:放入干燥的石蕊纸条; 乙:放入湿润的石蕊纸条; 向甲、乙处倒入CO2 | ________ | 二氧化碳能与水反应 |
D | 比较________ | 甲:放入一小粒高锰酸钾; 乙:放入一小粒碘; 向甲、乙处加入等量蒸馏水 | 甲中固体溶解形成紫色溶液; 乙中固体几乎不溶解 | 相同条件下,高锰酸钾在水中的溶解能力比碘强 |
查看答案和解析>>
科目:初中化学 来源:2020年江苏省无锡市宜兴市中考一模化学试卷 题型:实验题
过氧化钙晶体(CaO2·nH2O)常温下为白色,能溶于酸,难溶于水、乙醇,是一种温和的氧化剂,常用于鱼类长途运输的增氧剂等。
l.过氧化钙晶体(CaO2·nH2O)的制备
实验室制备过氧化钙晶体反应方程式为CaCl2+H2O2+2NH3+nH2O=CaO2?nH2O+2NH4Cl,实验装置如图。
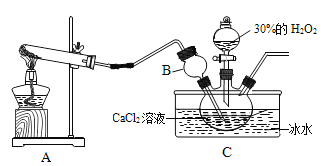
(1)装置A中生成的气体为______。
(2)装置B的作用是________。
(3)装置C采用冰水浴控制温度在0℃左右,可能的原因主要有:
①该反应是放热反应,温度低有利于提高CaO2?nH2O产率;
②____。
(4)反应结束后,经过滤、洗涤、低温烘干可获得CaO2?nH2O。检验晶体已洗涤干净的方法为______。
Ⅱ.过氧化钙晶体(CaO2?nH2O)中n的测定
资料:CaO2?nH2O加热至120℃完全失去结晶水,继续加热至350℃,剩余固体受热分解放出O2;
(5)某兴趣小组称取2.16g CaO2?nH2O样品,用热分析仪对其进行热分解实验,测得剩余固体的质量随温度变化曲线如图所示
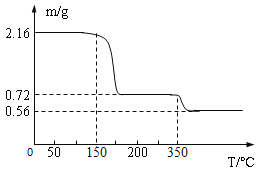
①CaO2?nH2O中n的值为____。(写出计算过程)
②350℃发生反应的化学方程式为_________。
③若过氧化钙品体中混有杂质(杂质不参加反应),会导致测得的n的值___(填“偏大”“偏小”或“不变”)。
Ⅲ.过氧化钙晶体(CaO2?nH2O)的性质研究
(6)该兴趣小组另称取少量CaO2?nH2O样品于试管中,加入适量的稀盐酸使样品完全反应,然后加入足量的Na2CO3溶液,看到_____现象,说明CaO2?nH2O与稀盐酸反应生成了CaCl2。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com