

分析 (1)氯化钡能和硫酸钠反应生成硫酸钡沉淀和氯化钠,从而除去硫酸钠;
(2)碳酸钠能够除去氯化钙和过量的氯化钡,操作不当容易导致最终得到的氯化钠不纯;
(3)过滤可以把反应生成的沉淀除去,从而使沉淀和溶液分离;
(4)稀盐酸能和氢氧化钠、碳酸钠反应,从而除去滤液中过量的氢氧化钠和碳酸钠.
解答 解:(1)氯化钡和硫酸钠反应的化学方程式为:BaCl2+Na2SO4=BaSO4↓+2NaCl.
故填:BaCl2+Na2SO4=BaSO4↓+2NaCl.
(2)加入碳酸钠溶液可以除去氯化钙和过量的氯化钡,碳酸钠和氯化钡顺序颠倒时,过量的氯化钡无法除去,最后所得的精盐水中会含有氯化钡.
故填:除去氯化钙和过量的氯化钡;BaCl2.
(3)通过操作Ⅰ可以把产生的沉淀和溶液分离.
故填:过滤.
(4)向滤液中滴加适量稀盐酸时,稀盐酸能和过量的氢氧化钠、碳酸钠反应,从而除去氢氧化钠和碳酸钠,得到不含有杂质的氯化钠溶液.
故填:除去滤液中过量的氢氧化钠和碳酸钠.
点评 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,有助于提高观察实验、进行实验的能力.


 习题精选系列答案
习题精选系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生铁比纯铁硬,故黄铜比纯铜硬 | |
| B. | CO有毒,故CO2也有毒 | |
| C. | 金刚石很硬,故石墨也很硬 | |
| D. | 氢氧化铝可治疗胃酸过多,故氢氧化钠也可治疗胃酸过多 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 如表是KNO3在不同温度时的溶解度,请回答下列问题.
如表是KNO3在不同温度时的溶解度,请回答下列问题.| 温度℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度(g) | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 日常生活中接触的金属材料,大多属于合金.其中黄铜是以锌作主要添加元素的铜合金.已知组成某弹壳的黄铜中只含有锌和铜,现将22g该弹壳碾成粉末后放入盛有足量的稀硫酸烧杯中,测得反应过程中生成的氢气的质量(单位为g)与反应时间(单位为min)的关系如图所示.试计算:
日常生活中接触的金属材料,大多属于合金.其中黄铜是以锌作主要添加元素的铜合金.已知组成某弹壳的黄铜中只含有锌和铜,现将22g该弹壳碾成粉末后放入盛有足量的稀硫酸烧杯中,测得反应过程中生成的氢气的质量(单位为g)与反应时间(单位为min)的关系如图所示.试计算:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
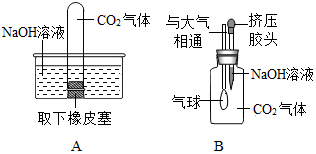 某兴趣小组同学将CO2分别通入澄清石灰水和氢氧化钠溶液中,观察到前者变浑浊,后者无明显现象.
某兴趣小组同学将CO2分别通入澄清石灰水和氢氧化钠溶液中,观察到前者变浑浊,后者无明显现象.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 太阳能电动车是在电动车的基础上,将太阳能转化成电能对车进行供电的,在很大程度上降低了电动车的使用成本,及时有效地补充电动车野外行驶途中的电量.请回答下列相关问题:
太阳能电动车是在电动车的基础上,将太阳能转化成电能对车进行供电的,在很大程度上降低了电动车的使用成本,及时有效地补充电动车野外行驶途中的电量.请回答下列相关问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 向12.2克碳酸钠和硫酸钠的混合物加入一定质量的稀硫酸后恰好完全反应,测得反应前后烧杯和所盛物质的总质量(m)与反应时间(t)的关系如图.其中烧杯的质量为30克(已知Na2CO3+H2SO4═Na2SO4+H2O+CO2↑).试计算:
向12.2克碳酸钠和硫酸钠的混合物加入一定质量的稀硫酸后恰好完全反应,测得反应前后烧杯和所盛物质的总质量(m)与反应时间(t)的关系如图.其中烧杯的质量为30克(已知Na2CO3+H2SO4═Na2SO4+H2O+CO2↑).试计算:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
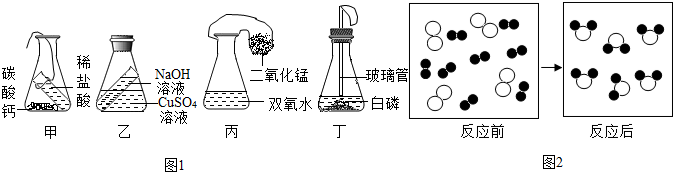
 粒子,请根据图示写出一个符合条件的化学方程式2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
粒子,请根据图示写出一个符合条件的化学方程式2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com