
| A. | KMnO4中K元素被氧化 | |
| B. | KMnO4中O元素被还原 | |
| C. | K2MnO4和MnO2是发生还原反应后的生成物 | |
| D. | 此反应不属于氧化还原反应 |
分析 反应中Mn元素化合价由+7价分别降低为+6价、+4价,KMnO4为氧化剂,K2MnO4、MnO2为还原产物,O元素化合价升高,O2为氧化产物,以此解答该题.
解答 解:A.反应中K元素化合价不变,KMnO4中K元素没被氧化,故错误;
B、O元素化合价升高,O2为氧化产物,KMnO4中O元素被氧化,故错误;
C、反应中Mn元素化合价由+7价分别降低为+6价、+4价,KMnO4为氧化剂,K2MnO4、MnO2为还原产物,故正确;
D、有元素化合价升降的反应是氧化还原反应,该反应中高锰酸钾中锰元素的化合价为+7价,二氧化锰中锰元素的化合价为+4价;氧气属于单质,氧元素的化合价为0,氧元素的化合价由-2价变0价;有元素化合价升降,属于氧化还原反应,故错误.
故选C.
点评 本题难度不大,理解有元素化合价升降的反应是氧化还原反应,掌握分解反应的特征、氧化物的特征、常见的原子团等是正确解答本题的关键.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 给试管中的液体加热,试管中的液体体积一般不超过试管容积的$\frac{1}{2}$ | |
| B. | 取液后的滴管不能倒置,但可平放 | |
| C. | 在无药量说明的情况下,某同学取用稀硫酸时,量取了2毫升 | |
| D. | 若取用的药品没有腐蚀性(如铁钉)可以用手拿 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 物质发生物理变化时一定伴随化学变化 | |
| B. | 物质发生化学变化是一定伴随物理变化 | |
| C. | 物质发生化学变化时可能伴随物理变化 | |
| D. | 二者之间没有任何关系 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
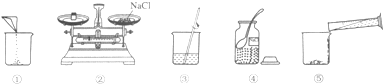 如图是配置氯化钠溶液的实验操作:
如图是配置氯化钠溶液的实验操作:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
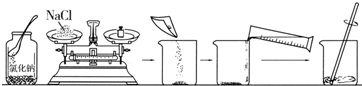
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com