解:(1)稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;图中没有用玻璃棒搅拌.
(2)铁生锈的两个条件是有水和空气,一段时间后,铁丝生锈变红,消耗掉试管内的氧气,试管内气体压强变小,U型管中水被外界大气压压入,所以a液面上升,b液面下降.
(3)C的实验操作的名称是过滤;标号c的仪器名称是漏斗;过滤是将不溶于水的固体与液体分离的一种方法,①从NaCl溶液中得到NaCl晶体可以采用蒸发结晶的方法;②Na
2CO
3、KCl均易溶于水,不能用过滤的方法分离;CaCO
3不溶于水,可用过滤的方法与水分离.
(4)镁在氧气中燃烧生成氧化镁,反应的化学方程式为:2Mg+O
2
2MgO.
故答案为:(1)没有用玻璃棒搅拌;(2)铁丝表面变红,U型管中a液面上升,b液面下降;(3)过滤;漏斗;③;(4)2Mg+O
2
2MgO.
分析:(1)根据浓硫酸的稀释方法进行分析解答.
(2)根据铁生锈的原理进行分析解答.
(3)根据过滤操作的原理、方法、注意事项等进行分析解答.
(4)D实验是镁在氧气中燃烧,写出反应的化学方程式即可.
点评:本题难度不大,掌握浓硫酸的稀释、铁生锈的原理、过滤操作、化学方程式的书写等是正确解答本题的关键.

 2MgO.
2MgO. 2MgO.
2MgO.




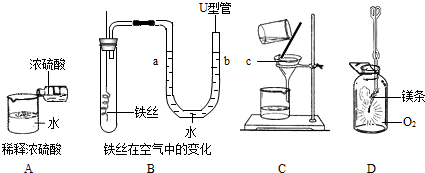
 (2013?宝坻区二模)以下是初中化学的一些基本实验:
(2013?宝坻区二模)以下是初中化学的一些基本实验: