
【题目】学习了二氧化锰过氧化氢分解有催化作用的知识后,某兴趣小组的同学提出问题:氧化铁能否起到类似于二氧化锰的催化作用呢?于是他们进行了以下探究.
(猜想)
Ⅰ.氧化铁不是反应的催化剂、也不参与反应,质量和化学性质反应前后均不变;
Ⅱ.氧化铁参与反应产生氧气,反应前后质量不变,但化学性质发生了改变;
Ⅲ.氧化铁是反应的催化剂,反应前后_____.
(实验)用天平称0.2g氧化铁,用试管取5mL 5%的过氧化氢溶液,进行如下实验:
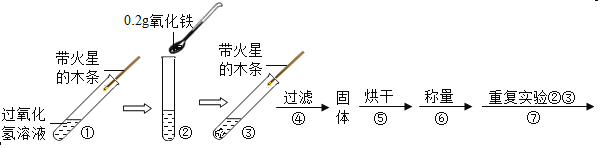
(注:氧化铁不溶于水,过滤可与水分离)
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
带火星的木条复燃. | _____ | 过氧化氢溶液中:_____ | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立. |
(2)步骤①的目的是_____.
(3)写出上述有关过氧化氢分解的文字表达式_____.
(4)步骤⑦重复实验②、③的目的是_____.
(继续探究)从上述实验得出氧化铁是反应的催化剂.对同种催化剂,有哪些因素可能影响催化效果?请提出猜想并设计实验进行探究._____(注意:至少探究两种因素,答对一种因素奖励2分,本題最多奖励4分,化学试卷总分不超过60分)
【答案】质量和化学性质都不变 0.2g 过氧化氢溶液中:产生气泡 检验过氧化氢能否自发分解 过氧化氢![]() 水+氧气 检验氧化铁在反应前后化学性质是否改变 猜想1:催化剂表面积大小影响化学反应的速率;
水+氧气 检验氧化铁在反应前后化学性质是否改变 猜想1:催化剂表面积大小影响化学反应的速率;
实验方法:取两支试管,分别加入5mL5%的过氧化氢溶液,再分别加入0.2g粉末状、颗粒状的氧化铁,观察产生气泡的快慢;
猜想2:催化剂的用量影响化学反应的速率;
实验方法:取两支试管,分别加入5mL5%的过氧化氢溶液,再分别加入0.2g、0.5g粉末状的氧化铁,观察产生气泡的快慢
【解析】
过氧化氢在二氧化锰做催化剂条件下分解生成水和氧气。催化剂在反应前后质量不变,化学性质不变。
根据前面两个猜想Ⅰ氧化铁不是反应的催化剂、也不参与反应,质量和化学性质反应前后均不变;Ⅱ氧化铁参与反应产生氧气,反应前后质量不变,但化学性质发生了改变;要和前面两个猜想形成比较,故Ⅲ氧化铁是反应的催化剂,反应前后质量和化学性质都不变。
[实验]
(1)填表如下所示:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
带火星的木条复燃. | 0.2g | 过氧化氢溶液中:产生气泡 | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立. |
(2)步骤①的目的是检验过氧化氢能否自发分解。
(3)过氧化氢分解生成水和氧气,文字表达式为![]() 。
。
(4)步骤⑦重复实验②、③的目的是检验氧化铁在反应前后化学性质是否改变。
[继续探究]
猜想1:催化剂表面积大小影响化学反应的速率。
实验方法:取两支试管,分别加入5mL5%的过氧化氢溶液,再分别加入0.2g粉末状、颗粒状的氧化铁,观察产生气泡的快慢。
猜想2:催化剂的用量影响化学反应的速率。
实验方法:取两支试管,分别加入5mL5%的过氧化氢溶液,再分别加入0.2g、0.5g粉末状的氧化铁,观察产生气泡的快慢。


科目:初中化学 来源: 题型:
【题目】工业上粗盐(含MgCl2、CaCl2、Na2SO4等杂质),精制的工艺流程如下:
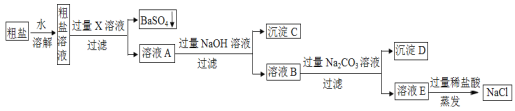
(1)X中含有的阳离子是________________;沉淀C的化学式是_____________。
(2)写出生成沉淀D的一个化学方程式_______________________________________。
(3)溶液E中加过量稀盐酸的作用是________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学城中学一化学兴趣小组选用如图所示装置,进行CO2的制取和性质实验,请你根据所学知识,依图回答下列问题:
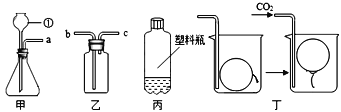
(1)写出图中仪器①的名称_______。
(2)装置甲中反应的化学方程式为_______。
(3)用装置乙排空气收集二氧化碳,验满时,燃着木条应放在_______ (填“b”或“c”)端。
(4)用图丙所示的质地较软的塑料瓶收集满CO2,再倒入一定量的紫色石蕊溶液,立即旋紧瓶盖,振荡,观察到的现象是_______。
(5)往图丁的烧杯内缓缓通入CO2,超薄材料做成的内充空气的气球会慢慢浮起,由此得出CO2具有的性质是_______。
(6)实验结束后,甲装置中仍然有固体,写出该装置中溶液里含有的微观粒子符号_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是元素周期表的另一种画法﹣﹣塔式周期表,在上面标有部分族序数及部分元素,请回答下列问题:

(1)图①中元素X对应图②中的_____是同种元素(填图②中的字母序号)。
(2)图②中,A粒子在反应中容易得到1个电子,形成的粒子符号为_____;图②中属于同一族的元素是_____(填图②中的字母序号)。
(3)已知一种化合物由离子构成且甲、乙、丙、丁四份不同浓度的该物质的水溶液中的离子个数如图③所示,该物质的化学式为_____(填字母)
A CaCl2 B NaCl C CuSO4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学科技小组同学将13.9g含杂质的纯碱样品(碳酸钠与氯化钠的混合物)
与90.5g稀盐酸相混合充分反应,测得反应生成气体的质量(m)与反应时间(t)的数据如下表所示:(已知:Na2CO3 +2HCl=2NaCl+CO2↑+H2O)
反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
气体质量m/g | 0 | 0.88 | 1.76 | 2.64 | 3.52 | 4.4 | 4.4 |
根据题目要求,回答下列问题:
(1)碳酸钠完全反应后,生成CO2的质量为_____g
(2)请根据表中数据在下面的坐标图中,画出反应是生成气体的质量(m)随时间(t)变化的曲线。____
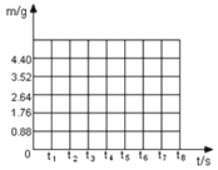
(3)求纯碱样品中Na2CO3的质量_____。
(4)反应结束后,溶液中没有剩余固体,则完全反应后溶液中NaCl的质量分数为_____;若要将反应得到的溶液的浓度稀释为10%,则需加入_____g的蒸馏水。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】目前世界上60%的镁是从海水中提取的。其主要步骤如下:
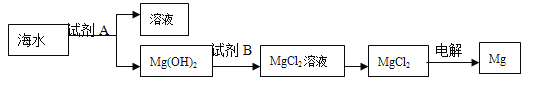
(1)提取镁的过程中,试剂A选用__________,试剂B选用________,由MgCl2制取镁的化学方程式为_____________。
(2)分离出Mg(OH)2后的NaCl溶液中还含有CaCl2、Na2SO4等杂质,为了获得纯净的NaCl溶液,在分离后的溶液中依次加入过量的BaCl2溶液、Na2CO3溶液,过滤,再向溶液中加入适量盐酸。实验中加入过量BaCl2溶液是为了除去__________,加入过量Na2CO3溶液的目的是________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质在水中的溶解度曲线。下列说法错误的是( )
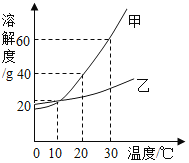
A. 10℃时,甲、乙两种物质的饱和溶液中溶质的质量相同
B. 蒸发溶剂可使接近饱和的乙溶液变成饱和溶液
C. 30℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为80g
D. 10℃时,将两种饱和溶液升温至30℃,溶液中溶质的质量分数都增大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入NaOH
溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示
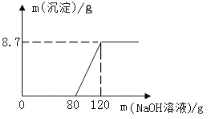
(1)计算氢氧化钠溶液的溶质质量分数;(要求写出计算过程)
(2)与氢氧化钠溶液反应所消耗硫酸溶质的质量为 克。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com