
分析 根据氢气的质量可以计算单质镁的质量、硫酸的质量、生成的硫酸镁的质量,从而可以计算出稀硫酸中硫酸的质量分数、所得溶液中溶质的质量分数.
解答 解:设镁的质量为x,稀硫酸中硫酸的质量为y,生成的硫酸镁的质量为z
Mg+H2SO4=MgSO4 +H2↑
24 98 120 2
x y z 0.4g
$\frac{24}{x}=\frac{98}{y}=\frac{120}{z}=\frac{2}{0.4g}$
x=4.8g,y=19.6g,z=24g
(1)稀硫酸中硫酸的质量分数是:$\frac{19.6g}{98g}×100%$20%;
(2)反应后所得溶液中溶质的质量分数是:$\frac{24g}{98g+4.8g-0.4g}×100%$=23.4%.
答:稀硫酸中硫酸的质量分数是20%;
反应后所得溶液中溶质的质量分数是23.5%.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


科目:初中化学 来源: 题型:解答题
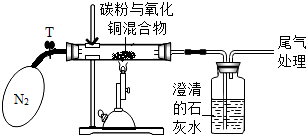 某小组同学对木炭还原氧化铜实验进行如下探究活动.
某小组同学对木炭还原氧化铜实验进行如下探究活动.| 木炭与氧化铜的质量比 | 1:7 | 1:11 | 1:13 |
| 实验现象 | 红热,产生大量气泡,石灰水变浑浊 | 红热,产生大量气泡,石灰水变浑浊 | 偶尔红热,有气泡,石灰水变浑浊 |
| 实验结果 | 表层铜珠较大,有较多黑色粉末 | 亮红色金属光泽,网状铜块 | 暗红色层状粉末里含微细铜粒 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
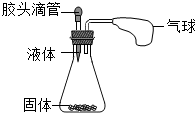 请用所学化学知识解释下列原理.
请用所学化学知识解释下列原理.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | t1℃时,三种物质的溶解度大小顺序为:丙>乙>甲 | |
| B. | t2℃时,甲、丙两种物质的溶液中溶质的质量分数相等 | |
| C. | 若要将组成在N点的甲溶液转变为M点的甲溶液,可以采用增加溶质的方法 | |
| D. | 将t3℃时甲、乙、丙三种物质的饱和溶液降温至t2℃,所得溶液溶质质量分数关系是乙>甲>丙 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com