
【题目】在日常生活中我们经常会使用金属材料.
(1)铝及其合金常用作于高压电缆,主要利用了铝优良的____.
(2)铝在空气中容易形成一层致密的氧化膜,从而保护铝不会进一步地被氧化.请用化学方程式表示该氧化膜的形成过程_____.
(3)不锈钢是生活中常用的合金,不锈钢的主要成分有铁、铬、镍.其中,铬的金属活动性与铁相近,常见化合价为+3、+6和+2,回答以下与金属铬(Cr)相关的问题.
①铬+3价的氧化物化学式为Cr2O3,读作_____.
②将铬丝插入下列溶液没有明显现象的是_____(填序号)
A AgNO3溶液 B H2SO4溶液 C NaCl溶液 D NaOH溶液
③CrCl3水溶液呈深绿色,它由深绿色难溶于水的氢氧化铬Cr(OH)3与盐酸作用制得.写出上述制取CrCl3的化学方程式______,预测反应现象______.
【答案】导电性 ![]() 三氧化二铬 CD
三氧化二铬 CD ![]() 深绿色固体消失,溶液呈深绿色
深绿色固体消失,溶液呈深绿色
【解析】
(1)铝及其合金常用作于高压电缆,主要利用了铝优良的导电性;故填:导电性;
(2)铝的化学性质比较活泼,在常温下,能与空气中的氧气反应,在其表面形成一层致密的氧化铝薄膜,故该反应的化学方程式为:![]() ;
;
(3)①由两种元素组成的化合物的名称一般读作某化某,故Cr2O3读作三氧化二铬,故填:三氧化二铬;
②A、铬的金属活动性与铁相近,因此比银的活动性强,可以置换出银,在铬的表面产生银白色的金属,不符合题意;
B、铬的金属活动性与铁相近,因此位于氢前,能够和稀硫酸反应产生氢气,观察到有气泡产生,不符合题意;
C、铬的活动性和铁相近,因此比钠的活动性弱,不能和氯化钠发生置换反应,无现象,符合题意;
D、金属铬不能和碱溶液发生反应,因此无明显现象,符合题意;
故选CD;
③氢氧化铬Cr(OH)3与盐酸反应生成三氯化铬和水,该反应的化学方程式为:![]() ; 氢氧化铬为深绿色固体,三氯化铬是深绿色的溶液,故实验现象为:深绿色固体消失,溶液呈深绿色。
; 氢氧化铬为深绿色固体,三氯化铬是深绿色的溶液,故实验现象为:深绿色固体消失,溶液呈深绿色。


科目:初中化学 来源: 题型:
【题目】实验室有一瓶含有K2CO3和K2SO4的混合溶液,某化学兴趣小组设计实验来测定溶质的质量分数。他们经过讨论后设计了如下装置进行实验探究:
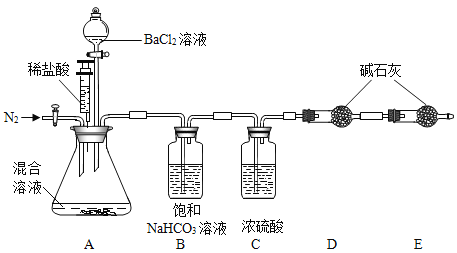
a.按图组装仪器,检查气密性,把100g混合溶液加入锥形瓶中装好药品;
b.打开A中活塞,通入N2一段时间,再关闭活塞,称D装置质量m1克;
c.逐滴加入BaCl2溶液至不再产生沉淀;关闭分液漏斗,再用针筒打入稀盐酸,至不再产生气体,实验过程中测得锥形瓶中沉淀的数据如下图;
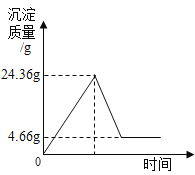
d.打开A中活塞,缓缓通一会儿N2。
e.再称得D装置的质量为m2克;
请你根据题意回答下列问题:
(1)24.36g沉淀中含有什么物质(填化学式)_____,针筒注入稀盐酸产生气体的方程式:_____。
(2)求原混合液中K2SO4的质量分数_____。
(3)小明略加思考后说,通过D装置的质量变化可以求出混合溶液中K2CO3的质量分数,结果_____(填“偏大”、“不变”或“偏小”),理由_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2018年10月,中科院大连化物所与福州大学化学学院合作发展了一种固态Z一机制复合光催化剂,实现了太阳能人工光合成燃料过程,反应的微观示意图如图所示:
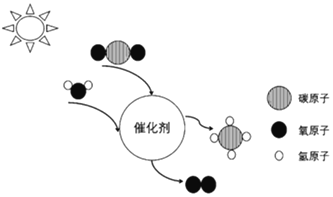
(1)该转化过程中,______(填“原子”或“分子”)没有发生变化,化合价升高的元素是______。
(2)写出该过程的化学方程式______。
(3)两种反应物的质量比为______。
(4)该过程可缓解______,是人类解决环境问题的途径之一。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)写出你家中的任一生活必需品,它可能含有哪些化学元素?
必需品_____,可能含有的化学元素_____。
(2)请利用所学的化学知识回答。
①铅笔芯粉末因为含有_____,有滑腻感,可做家庭锁头的润滑剂;
②油锅着火,通常盖上锅盖,灭火的原理是_____;
③冬季是“煤气中毒”的高发季节,使人中毒的主要气体是_____,预防中毒的措施是_____。
(3)盐酸中滴入紫色石蕊试液时显_____色,滴入无色酚酞时显无色;打开盛有浓盐酸的试剂瓶盖,可以看到瓶口有_____产生,这说明浓盐酸具有_____性。盐酸常用于金属表面除锈,有关反应的化学方程式为_____。氢氧化钠溶液中滴入紫色石蕊试液时显_____色,滴入无色酚酞时显_____色。稀释浓硫酸时,要把_____缓缓地沿器壁注入_____中,同时用玻璃棒不断搅拌,以使热量及时地扩散。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验能达到实验目的的是( )
A. 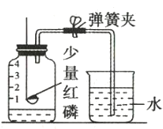 探究空气中氧气含量
探究空气中氧气含量
B. 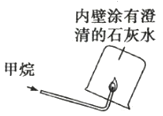 验证甲烷(CH.4)燃烧生成二氧化碳和水
验证甲烷(CH.4)燃烧生成二氧化碳和水
C.  探究反应物浓度对反应速率的影响
探究反应物浓度对反应速率的影响
D.  探究分子运动
探究分子运动
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是KNO3和NaCl的溶解度曲线,以下说法不正确的是( )
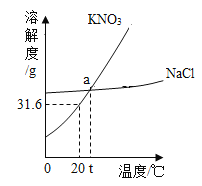
A.a点表示的含义:t℃,KNO3和NaCl的溶解度相等
B.KNO3饱和溶液中含有少量的NaCl,可采用降温结晶法提纯KNO3
C.20℃,向50 g水中加入16 g KNO3,可得到66 g KNO3溶液
D.将t℃时两种物质的饱和溶液降温到20℃,所得溶液的质量分数NaCl大于KNO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酸、碱、盐参与的化学反应有一定的规律。
(1)取少量氢氧化钠溶液于烧杯中,滴入几滴酚酞试液,在搅拌下,再逐滴加入稀盐酸至溶液变成无色,此时溶液的pH较之前_____(填“升高”“降低”或“不变”),若用实验证明酚酞仍存在于溶液中,你的实验操作方法是_____,现象是_____。
(2)已知反应:酸(稀)+X→CuSO4+水,若X为金属氧化物,该反应的化学方程式是_____;若该反应为中和反应,则X物质是_____。
(3)CuSO4溶液不宜用铁制容器盛装,原因是_____(用化学方程式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于数字含义的解释中,正确的是( )
A.Zn2+中的“2”表示锌原子得到2个电子
B.H2O中的“2”表示一个水分子中含有2个氢元素
C.2NO中的“2”表示2个一氧化氮分子
D.![]() 中化学式上方的“+3”表示2个铝的化合价为+3价
中化学式上方的“+3”表示2个铝的化合价为+3价
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学研究小组的同学对金属铁、铝、铜进行系列研究。
(1)合金的应用是人类社会文明发展的象征。有下列三种合金:①铁合金;②铝合金;③铜合金,这三种合金被广泛应用的先后顺序按年代由远及近排列应是_______。
(2)该小组的同学利用单质铜制取 Cu(OH)2,其设计方案如图 1:
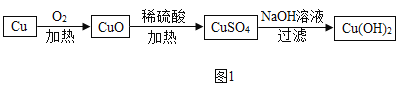
①铜在受热转化为 CuO 的过程中,观察到的现象是_____________。
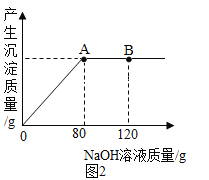
②取一定量的 CuO 放入盛有一定量稀硫酸的烧杯中,恰好完全反应。向烧杯中逐滴加入 10%的 NaOH 溶液,产生沉淀的质量与所滴入 NaOH 溶液质量的关系曲线如图 2 所示。当滴入 10%的 NaOH 溶液 120g 时(即 B 点),试通过计算,求此时所得 Cu(OH)2沉淀的质量_______。(计算结果精确至 0.1g)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com