
| ||
| △ |
| 245 |
| x |
| 96 |
| 4.8g |


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
| A、它是纯天然饮品,不含任何化学物质 |
| B、它是一种硬水 |
| C、它在通电条件下不能分解成氢气和氧气 |
| D、它纯净、清洁,但不宜长期饮用 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、我们应珍惜化石燃料,因为它们既是燃料,又是重要的化工原料,且不可再生 |
| B、在合理使用化石燃料的同时,我们应努力寻求开发新能源 |
| C、国家决定推广乙醇汽油的应用,乙醇汽油是一种新型化合物 |
| D、汽车使用乙醇汽油能减少有害气体的排放 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
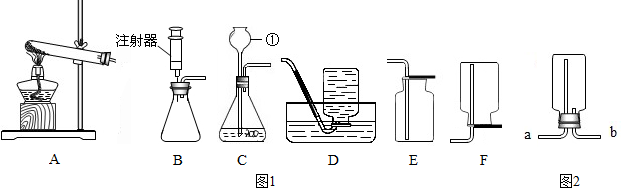
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com