
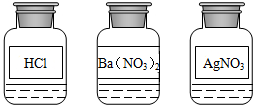 实验室中有一瓶标签破损的固态铵盐,它可能是NH4Cl、NH4NO3、NH4HCO3、(NH4)2SO4中的一种,请利用如图所示的溶液进行实验探究.
实验室中有一瓶标签破损的固态铵盐,它可能是NH4Cl、NH4NO3、NH4HCO3、(NH4)2SO4中的一种,请利用如图所示的溶液进行实验探究.科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
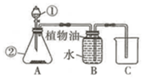 如图是小华同学设计的气体制取和收集装置,请你和他一起回答下列问题:
如图是小华同学设计的气体制取和收集装置,请你和他一起回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 发现家中燃气泄露,及时打开排气扇 | |
| B. | 炒菜时油锅着火用锅盖盖灭 | |
| C. | 乘坐公共交通工具时严禁携带易爆品 | |
| D. | 火场逃生时在有烟雾的地方捂住口鼻匍匐前进 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
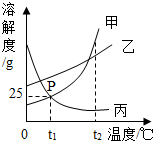
| A. | P点表示甲、丙两种物质的饱和溶液质量相等 | |
| B. | t1℃时,乙物质的饱和溶液,升温至t2℃时仍是饱和溶液 | |
| C. | t1℃时,甲物质的饱和溶液中溶质和溶剂的质量比为1:4 | |
| D. | 将三种物质的溶液从t2℃降至t1℃,溶质质量分数最小的一定是丙物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
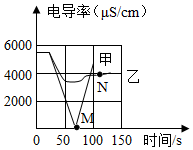 某化学兴趣小组通过探究活动学习和理解化学知识.请你一起研究学习,并回答有关问题.
某化学兴趣小组通过探究活动学习和理解化学知识.请你一起研究学习,并回答有关问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com