
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 太阳能电动车是在电动车的基础上,将太阳能转化成电能对车进行供电的,在很大程度上降低了电动车的使用成本,及时有效地补充电动车野外行驶途中的电量.请回答下列相关问题:
太阳能电动车是在电动车的基础上,将太阳能转化成电能对车进行供电的,在很大程度上降低了电动车的使用成本,及时有效地补充电动车野外行驶途中的电量.请回答下列相关问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 去除杂质的方法 |
| A | NaCl(Na2CO3) | 加入足量盐酸、蒸发结晶 |
| B | CaCl2(CaCO3) | 加入足量的水、过滤、结晶 |
| C | Fe2(SO4)3(H2SO4) | 加入足量的铁、过滤、结晶 |
| D | MgSO4(H2SO4) | 加入足量的氧化镁、过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水在固态时分子是静止不动的 | |
| B. | 水结冰后体积变大是水分子的体积增大造成的 | |
| C. | 水由液态变成气态时水分子质量变小 | |
| D. | 保持水的化学性质的微粒是水分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
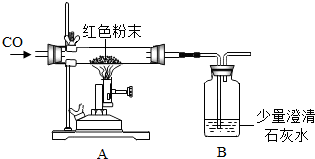 在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与探究并回答问题.
在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究.请你参与探究并回答问题.| 反应前 | 反应后 | |
| Ⅰ 组 | 玻璃管和红色粉末的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
| Ⅱ 组 | 洗气瓶和所盛溶液 的总质量为180.0g | 洗气瓶和瓶中物质 的总质量为183.1g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com