
【题目】实验室使用块状石灰石(CaCO3)和稀盐酸制CO2,当观察不到有气泡产生,固体仍有剩余时,通常认为反应结束,剩余液呈中性。某兴趣小组对此进行了以下探究:
【实验操作】(1)向试管中加入5粒石灰石,倾倒约试管体积1/3的稀盐酸(1:1);观察不到气泡后,仍有固体剩余;将试管静置。
(2)取上层清液,用pH试纸测得溶液pH=2,说明溶液显酸性;
【实验思考Ⅰ】反应剩余液中有哪些物质?其中能使溶液pH=2的有哪些?
【实验探究Ⅰ】(1)甲同学通过实验排除了CaCl2的可能性。简述其实验方案___________。
(2)乙同学将CO2通入蒸馏水中至饱和,测得pH>5,。
(3)综合甲、乙两同学实验,得出的结论是:剩余液中还含有_______________。
【实验思考Ⅱ】试管中剩余固体是否仍含有CaCO3?
【实验探究Ⅱ】小组同学向试管中继续加入稀盐酸(1:1),又有大量气泡产生。
(1)由此得出的结论是_____________________________,写出该反应的化学方程式
比较稀盐酸加入前后的实验现象,解释“又有大量气泡产生”的原因:________________________________________。
【拓展延伸】(1)反应剩余液放置一段时间后,溶液pH增大,其主要原因是盐酸有挥发性,溶质氯化氢挥发了。
(2)假如用100g14.6%的稀盐酸和足量的石灰石反应,看不到气泡产生时,停止收集气体。收集到的CO2质量_______(选填“>”、“<”、“=”)8.8g。
【答案】[实验探究I](1)另取CaCl2溶液,测得其显中性。(3)盐酸
[实验探究II](1)剩余固体中含有CaCO3CaCO3+2HCl==CaCl2+H2O+CO2![]()
(2)盐酸的浓度增大了,反应又能进行了
[拓展延伸]<
【解析】
试题分析:[实验探究I](1)另取CaCl2溶液,测得其显中性,排出氯化钙的可能性;
CO2通入蒸馏水中至饱和,测得pH>5,说明不是二氧化碳与水反应生成的碳酸的原因,故剩余液还有盐酸;
[实验探究II](1)小组同学向试管中继续加入稀盐酸(1:1),又有大量气泡产生,说明剩余固体中含有CaCO3,碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳:CaCO3+2HCl== CaCl2 +H2O+CO2![]() ;
;
(2)盐酸的浓度增大了,反应又能进行了;
【拓展延伸】由探究可知,当盐酸的浓度较低时,碳酸钙与盐酸不能继续反应,故最终生成的二氧化碳的质量小于8.8g。


科目:初中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.化合反应一定是氧化反应
B.有氧气参加的反应一定是化合反应
C.糖和水混合制成糖水是化合反应
D.化合反应是由两种或两种以上的物质生成另一种物质的反应,与是否有氧气参加无关
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)下列为实验室常用的实验装置,回答问题:
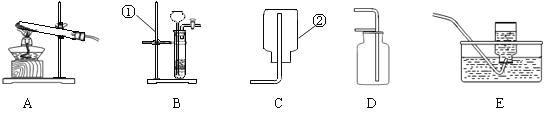
(1)写出带有标号仪器的名称:① ;② 。
(2)用锌和稀硫酸制取氢气,应选用的发生装置是 (填序号,下同),收集装置是 。
(3)实验室常用稀盐酸和石灰石反应制CO2,该反应的化学方程式 ;
此外,也可用加热碳酸氢钠(NaHCO3)固体(产物为碳酸钠、二氧化碳、水)来制取CO2,该反应的化学方程式 ,若用此法来制取CO2,应选用的发生装置为 ,收集装置为 。
(4)右图所示装置可用来测量生成的CO2的体积,其中在水面上放一层植物油的目的是 ,植物油上方原有的空气对实验结果 (填“有”或“无”)明显影响。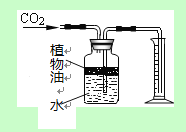
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列物质在氧气中燃烧的现象,正确的是( )
A.铁丝在氧气中燃烧火星四射,放热,生成黑色物质
B.红磷在氧气中燃烧产生白雾,放出大量的热
C.木炭燃烧生成二氧化碳,倒入瓶中的澄清石灰水变浑浊
D.硫燃烧发出淡蓝色火焰,放热,生成有刺激性气味的气体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线
相交于P点.据图回答:

(1)t2℃时30g a物质加入到50g水中不断搅拌,形成的溶液中溶质的质量分数是________.
(2)t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是________(填写物质序号).
(3)在t2℃时,将等质量的a、b、c三种物质的饱和溶液同时降温至t1℃时,析出晶体最多的是________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关化学知识的描述正确的是
A.催化剂不仅能改变化学反应速率,而且会增加生成物的质量
B.电解水时正极产生氢气,负极产生氧气,其体积比为2:1
C.NH4NO3是一种复合肥料,溶解时吸热
D.酸溶液加水稀释,溶液的pH会变大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂排放的废水中含有NaOH和Na2CO3,为了测定废水中NaOH的质量分数,取废水100g逐滴加入稀盐酸至过量,测得生成气体的质量与所加稀盐酸的质量关系如图所示。试计算:

(1)当所取样品完全反应时,生成气体的质量为 g。
(2)恰好完全反应时所得溶液的溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们发现将NaOH溶液和稀盐酸混合后没有明显现象,为了证明NaOH能与HCl发生中和反应,设计了如下实验:
实验步骤[ | 现象 | 结论 |
实验1.取少量NaOH溶液于试管中,向其中滴加几滴无色酚酞试液,振荡。 | 溶液呈_______色 | |
实验2.向实验1的试管中加入适量的稀盐酸,振荡。 | _______________。 | NaOH与HCl能反应。 |
![]()
【解释与结论】写出NaOH与HCl反应的化学方程式______________。
【反思与评价】同学们对实验2反应后所得溶液的酸碱性进行讨论,小玲同学认为呈碱性,小生同学认为呈中性,小柏同学认为也可能呈酸性,最后同学们否定了小玲同学的说法,其理由是___;欲进一步确定实验2反应后所得溶液的酸碱性,其操作是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com