
取久置于空气中已部分变质的CaO样品10.0 g,在高温下煅烧,将生成的气体全部通入202.16 g质量分数为3.0%的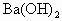 溶液中,过滤,得到的沉淀的质量为3.94 g.已知煅烧后的样品中只含一种固体物质,其质量为9.12 g.
溶液中,过滤,得到的沉淀的质量为3.94 g.已知煅烧后的样品中只含一种固体物质,其质量为9.12 g.
求:(1)样品中各物质的质量分数;
(2)滤液中溶质的质量分数.
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源:2010年专题突破训练:根据化学式的计算1(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com