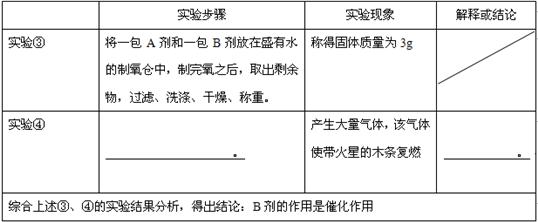
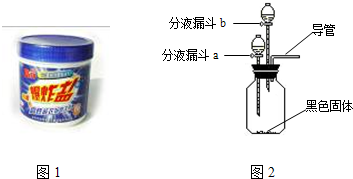
��������1���������������ɵ�װ������Ҫ���װ�õ������Խ��н��
��2������ϡ�����к���ˮ�����Թ�̼���ƣ���ѧʽxNa
2CO
3?yH
2O
2����ˮ�ֽ�Ϊ̼���ƺ������⣬ϡ�����̼���Ʒ�Ӧ���������ơ�ˮ�Ͷ�����̼����������Ͷ������̻������ˮ���������н��
��3�����ݼ�����Ҫ�ƾ����Լ�Ũ���������ˮ�Խ��н��
��4�����ݲ����ͨ��һ��ʱ��N
2��Ŀ���ǽ�װ���ڵĿ����ϳ�������ۼ���ͨ��N
2��Ŀ���������ɵ�����ͨ��װ��C��D������ܼ���ͨ��N
2��Ŀ���������ɵĶ�����̼������ȫ����װ��C��D���ս��н��
��5�����ݵ���ʼ�ղ���ˮ�е�Ŀ���Ƿ�ֹ����̼�ж���������������װ��C��D�Լ�����������ˮ���н��
��6������������ͭ��Ӧ��������ͭ���н��
��7������װ��A��������������ʱ˵����̼������ȫ��Ӧ���н��
��8������װ��C���ӵ������������ɶ�����̼��������װ��D���ӵ��������������������������н��
��9�����ݲ��
��ֵƫ��˵��������ʵ������в�ö�����̼������ƫ�����������������ƫС���н��
����⣺��1�����������ɵ�װ������Ҫ���װ�õ������ԣ�
������װ�õ������ԣ�
��2��ϡ�����к���ˮ����̼���ƣ���ѧʽxNa
2CO
3?yH
2O
2����ˮ�ֽ�Ϊ̼���ƺ������⣬����ϡ�����̼���Ʒ�Ӧ���������ơ�ˮ�Ͷ�����̼����������Ͷ������̻������ˮ��������������ƿ�еμ�ϡ���ᣬ�����������ж�����̼����������Ӧ���м�������MnO
2�������Ǽӿ��������ֽ��������������ʣ�
���������̼���������ӿ��������ֽ��������������ʣ�
��3��������Ҫ�ƾ��ƣ�����ȫ��װ��ȱ�ٵIJ��������Ǿƾ��ƣ�Ũ���������ˮ�ԣ�����װ��B���������������е�ˮ������
����ƾ��ƣ����������е�ˮ������
��4�������ͨ��һ��ʱ��N
2��Ŀ���ǽ�װ���ڵĿ����ϳ�������ۼ���ͨ��N
2��Ŀ���������ɵ�����ͨ��װ��C��D������ܼ���ͨ��N
2��Ŀ���������ɵĶ�����̼������ȫ����װ��C��D���գ�
�����װ���ڵĿ����ϳ��������ɵ�����ͨ��װ��C��D�������ɵĶ�����̼������ȫ����װ��C��D���գ�
��5������ʼ�ղ���ˮ�е�Ŀ���Ƿ�ֹ����̼�ж���������������װ��C��D������������ˮ�������жϵ���ͨ�����ʵ������ǿ��Թ���ð�����ݵĿ�����
�����ֹ����̼�ж���������������װ��C��D���ǿ��Թ���ð�����ݵĿ�����
��6��������ͭ��Ӧ��������ͭ����Ӧ�Ļ�ѧ����ʽΪ2Cu+O
22CuO��ʵ��ǰ������Ϊ��ɫ��ͭ˿��Ϊ��ɫ�����2Cu+O
22CuO����ɫ��ͭ˿��Ϊ��ɫ��
��7����װ��A��������������ʱ˵����̼������ȫ��Ӧ�����װ��A�������������ɣ�
��7��װ��C���ӵ������������ɶ�����̼��������������̼�����ʵ���=
=0.2mol��װ��D���ӵ����������������������������������ʵ���=
=0.15mol��������0.2mol������̼��Ҫ̼���Ƶ����ʵ���Ϊx������0.15mol������Ҫ������������ʵ���Ϊy��
Na
2CO
3+H
2SO
4�TNa
2SO
4+H
2O+CO
2��
1 1
x 0.2mol
x=0.2mol
2H
2O
22H
2O+O
2��
2 1
y 0.15mol
y=0.3mol
����̼���ƺ�����������ʵ���֮��=0.2mol��0.3mol=2��3���ʹ�̼���ƵĻ�ѧʽ2Na
2CO
3?3H
2O
2��
���2Na
2CO
3?3H
2O
2��
��8�����
��ֵƫ��˵��������ʵ������в�ö�����̼������ƫ�����������������ƫС������ԭ����������ɵ�����û��ȫ����ͭ��Ӧ��
������ɵ�����û��ȫ����ͭ��Ӧ��