


科目:初中化学 来源: 题型:
| 农作物 | 大豆 | 茶 | 玉米 | 甘草 | 马铃薯 |
| pH | 6.0~7.0 | 5.0~5.5 | 7.0~8.1 | 7.2~8.5 | 4.8~5.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | H2气体 | HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| B | NaCl溶液 | Na2CO3 | 加入稀硫酸至不再产生气泡 |
| C | CO气体 | CO2气体 | 通过灼热的Fe2O3 |
| D | CaCl2溶液 | HCl | 加入过量的碳酸钙、再过滤 加入过量的碳酸钙、再过滤 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2013?江西模拟)甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
(2013?江西模拟)甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
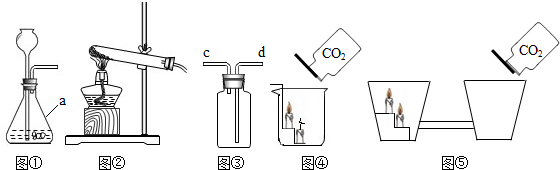
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| ①实验操作 | ②实验现象 |
| 剪下一片变黑的铜片,放入试管中,加入足量的 稀硫酸 稀硫酸 溶液.(填“稀硫酸”或“氢氧化钠溶液”) |
铜片表面的黑色物质全部消失,露出红色的铜,溶液变为 蓝色 蓝色 色. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com