
分析 根据浓硫酸、氢氧化钠的性质进行分析必须密封保存的原因;首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答 解:(1)长期敞口放置浓硫酸,因吸水性而导致浓度减小,因此浓硫酸常作为氧气、氢气、二氧化碳等气体的干燥剂;
(2)固体氢氧化钠必须密封保存,这是因为氢氧化钠具有吸水性,能吸收空气中的水分发生潮解;还能与空气中的二氧化碳反应生成碳酸钠和水,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O.
(3)碳酸氢铵在加热条件下生成氨气、水和二氧化碳,符合要求,反应的化学方程式为:NH4HCO3 $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O.
故填:(1)吸水性;氧气、氢气、二氧化碳;(2)潮解;CO2+2NaOH═Na2CO3+H2O;(3)NH4HCO3 $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O.
点评 本题难度不大,考查氢氧化钠的性质,熟练掌握浓硫酸的性质、氢氧化钠的性质等是正确解答本题的关键.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

 ,该原子在化学反应中易失(填“得”或“失”)电子,形成的离子符号为Al3+铜和稀硫酸不反应,与浓硫酸在一定条件下可以反应,其化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+X↑+2H2O,则X的化学式为SO2.
,该原子在化学反应中易失(填“得”或“失”)电子,形成的离子符号为Al3+铜和稀硫酸不反应,与浓硫酸在一定条件下可以反应,其化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+X↑+2H2O,则X的化学式为SO2.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 青铜是人类最早使用的合金 | |
| B. | 缺钙会引起骨质疏松 | |
| C. | 法国化学家拉瓦锡第一次明确提出空气是由氧气和氮气组成的 | |
| D. | “白色污染”是指白色建筑材料垃圾引起的污染 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | “稀释浓硫酸”实验中,将刚稀释得到的硫酸溶液转移至试剂瓶中 | |
| B. | “粗盐的初步提纯”实验中,过滤时将悬浊液直接倒入漏斗里 | |
| C. | “配制一定溶质质量分数的氯化钠溶液”实验中,药匙中多余的药品应放回原瓶 | |
| D. | “高锰酸钾制取氧气”实验中,收集好气体后应先将导管移出水槽再停止加热 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题


查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
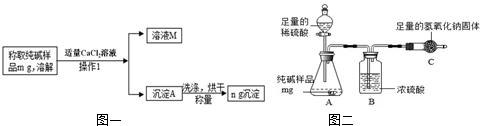
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com