
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加氯化钙溶液(或稀盐酸). | 产生白色沉淀(或有气泡冒出) | 该溶液是碳酸钠溶液. 有关反应的化学方程式为: CaCl2+Na2CO3═CaCO3↓+2NaCl(或Na2CO3+2HCl═2NaCl+H2O+CO2↑). |
分析 (1)分析测定溶液酸碱度的操作,指出其中的问题并判断对结果的影响;
(2)根据溶解度与饱和溶液的溶质质量分数的关系,由氢氧化钙常温下的溶解度进行判断;
(3)[进行实验]根据碳酸钠与稀硫酸或氯化钡溶液反应所出现的现象,完成检验碳酸钠的实验方案的填写;
[实验反思]①根据碳酸钠的性质,判断能与碳酸钠反应且有明显现象出现的碱,写出反应的化学方程式;
②根据节约药品的原则,评价对于无法辨认的药品的处理方法.
解答 解:(1)测定溶液的酸碱度时,不可把pH试纸用水湿润,这样测定的碱溶液的酸碱度会因加水稀释而偏小,但根据测得的酸碱度为10判断溶液呈碱性还是正确的;故选B;
(2)常温下氢氧化钙的溶解度为0.18g,其饱和溶液中溶质质量分数=$\frac{0.18g}{0.18g+100g}$×100%<0.18%,而该溶液溶质质量分数为10%,所以不可能是氢氧化钙;
(3)氯化钙和稀盐酸都可以用来鉴别氢氧化钠和碳酸钠,氯化钙与碳酸钠反应产生碳酸钙白色沉淀,方程式为CaCl2+Na2CO3═CaCO3↓+2NaCl,稀盐酸与碳酸钠反应产生二氧化碳气体,方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑;
[实验反思]①根据碳酸钠溶液与澄清石灰水混合可使溶液因生成碳酸钙沉淀而变浑浊的现象,利用氢氧化钙溶液检验碳酸钠,化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
②对于标签被腐蚀的试剂,本着节约原则,应尽可能确定药品的组成,不可随意扔弃,既不安全又造成浪费;故C不可取;
故答案为:
(1)常温下不可能得到质量分数为10%的氢氧化钙溶液;
(2)B;
(3)[进行实验]实验步骤:氯化钙溶液(或稀盐酸)
实验现象:产生白色沉淀(或有气泡冒出)
CaCl2+Na2CO3═CaCO3↓+2NaCl(或Na2CO3+2HCl═2NaCl+H2O+CO2↑)
[实验反思]①Ca(OH)2;Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;②C.
点评 本题根据氢氧化钠、氯化钠、氢氧化钙、碳酸钠几种物质的性质特点,采取“利用测定结果进行先排除,最后进行实验检验的”方法确定未知溶液,涉及对四种物质相关性质及变化规律的考查.


科目:初中化学 来源: 题型:选择题
| A. | 硫在氧气中燃烧,发出明亮的蓝紫色火焰 | |
| B. | 在空气中打开盛浓盐酸的试剂瓶瓶塞,产生白雾 | |
| C. | 在电解水实验中,与电源正负极相连的两极上产生的气体体积比约为2:1 | |
| D. | 取少量氢氧化钠固体露置在空气中,其表面潮湿并逐渐溶解 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
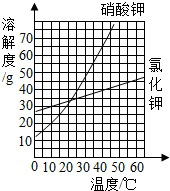 如图是氯化钾和硝酸钾两种固体溶解度曲线图.
如图是氯化钾和硝酸钾两种固体溶解度曲线图.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 活性炭的吸附性 石墨的润滑性 | |
| B. | 甲烷的可燃性 氧气的助燃性 | |
| C. | 浓盐酸的挥发性 碳酸的不稳定性 | |
| D. | 一氧化碳的还原性 金属的导电性 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 电解水实验说明水是由氢气和氧气组成 | |
| B. | 水变成水蒸气后体积变大是水分子的体积增大造成 | |
| C. | 水体有一定的自净功能,工业污水可直接排入河流 | |
| D. | 蒸馏能降低水的硬度 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 黄曲霉素的相对分子质量为312 | |
| B. | 黄曲霉素是一种有机物化合物 | |
| C. | 黄曲霉素中碳、氢、氧三种元素的质量比17:12:6 | |
| D. | 黄曲霉素是由碳、氢、氧三种元素组成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com