
���� ��1�������������������ܹ�ͬ˵����������Ҫ��ƽ�ⶼ����ԵĽ��н��
��2�������ڱ��͵�����ͭ��Һ�У�����һ������ͭ���壨�����������䣩���ܽ������Ȼ�������н��
��� �⣺��1�������������������ܹ�ͬ˵����������Ҫ��ƽ�ⶼ����Եģ������ı䣬ƽ�ⱻ�ƻ�����ѡ��C��
��2���ڱ��͵�����ͭ��Һ�У�����һ������ͭ���壨�����������䣩���ܽ������Ȼ�������У�ֻ������λʱ������ɢ����Һ�еĸ������Ӻʹ���Һ������ص��������ij������������ȣ������������������������£�����������ͭ��Һ�з���һ������ͭ���壬��һ��۲죬�ᷢ�־�����״�ı䡢�������䣮��ѡ��B��
���� ���⿼���ܽ�ƽ��Ĺ��ɺ��������ڻ���֪ʶ�Ŀ��飬�ѶȽ�С��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������Դ | B�� | ��ֹʹ��ú��ʯ�͵ȿ���ȼ�� | ||
| C�� | ʹ�õ綯�� | D�� | ���ӳ��е��̵���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
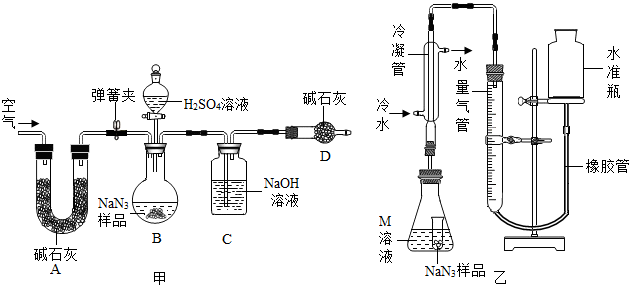
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Mg��Mg2������þԪ�� | B�� | �������ܴ� | ||
| C�� | Mg��Mg2��������Ų���ͬ | D�� | Mg�õ�2�����Ӻ��ܱ�ΪMg2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com