
下图为为氯化铵和硫酸钠的溶解度曲线。下列说法中不正确的是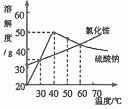
| A.40℃时,氯化铵、硫酸钠的溶解度相同 |
| B.氯化铵的溶解度随温度的升高而增大 |
| C.将50℃时硫酸钠的饱和溶液降低温度,始终有晶体析出 |
| D.将60℃时硫酸钠的饱和溶液降温至40℃,溶质的质量分数不变 |
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| △ |
| ||
| △ |
| ||
| 高温、高压 |

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| △ |
| ||
| △ |
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
某化学兴趣小组回收利用废旧干电池。
实验 1 回收填料中的二氧化锰和氯化铵
查阅资料:废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水。兴趣小组的同学们设计回收物质的流程如下图所示。
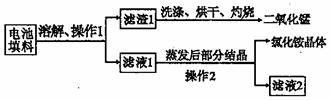 |
(1)操作 1 的名称是 ▲ ,该操作中玻璃棒的作用是 ▲ 。
(2)灼烧滤渣 l 的目的是  ▲ 。
▲ 。
(3)二氧化锰是氯酸钾受热分解的催化剂,下表是他们的有关实验数据,请你回答有关问题:
| 二氧化锰与氯酸钾的质量比 | 1/40 | 1/20 | 1/10 | 1/5 | 1/3 | 1/2 | 2/3 | 1/1 | 2/1 |
| 生成1L氧气所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
①据上表可知二氧化锰与氯酸钾的质量比为 ▲ 时,反应速率最快。分析可知反应前后二氧化锰在固体混合物中质量分数是 ▲ (“不变”或“变大”或“变小”)。
②二氧化锰的用量过少时产生氧气的速率很慢,原因是 ▲ ;二氧化锰用量过多,产生氧气的速率 ▲ (填“变快”、“变慢”或“不变”),通过分析可知,在化学反应中催化剂的用量 ▲ (填“是”或“不是”)越多越好。
实验 2 利用外壳回收物锌制取氢气及相关探究
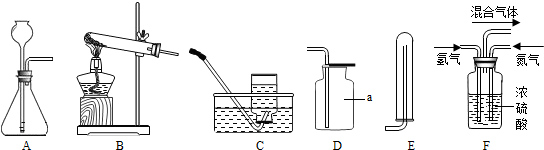
(4)用锌粒和稀硫酸可制取氢气(锌+硫酸→硫酸锌+氢气)。己知氢气密度比空气小且难溶于水,提供装置如下图:应选择:发生装置为 ▲ (填编号),排空气法收集装置为 ▲ (填编号)。
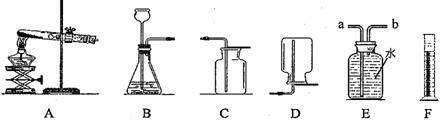
(5)探究影响锌与稀硫酸反应快慢的因素。反应过程中,用前 10 min 内收集的氢气体积比较反应的快慢。控制其他条件相同,进行下表四组实验,获得数据如下表。
| 验实 号编 | 试剂 | 前 10 min 内产生 的氢气体积(mL) | |
| 不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
| a | 纯锌 | 30 mL 30 % | 564.3 |
| b | 含杂质的锌 | 30 mL 30 % | 634.7 |
| c | 纯锌 | 30 mL 20 % | 449.3 |
| d | 纯锌 | 40 mL 30 % | 602.8 |
①比较实验 a 和实验 b ,可以得到的结论是 ▲ 。
②为了研究硫酸浓度对反应快慢的影响,需比较实验 ▲ 和实验 ▲ (填编号)。
③控制其他条件相同,需控制的条件是 ▲ (例举一种条件即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com