
| 实验步骤 | 实验现象 | 结论 |
| 先用pH试纸测定稀盐酸的pH,再逐渐滴加氢氧化钠溶液.并不断振荡,同时测定混合液的pH. | pH逐渐变大, 最后pH≥7 | 稀盐酸与氢氧化钠 溶液能发生反应 |
| 实验步骤 | 实验现象 | 结论 |
| 稀盐酸与氢氧化钠 溶液反应放热 |
| 实验步骤 | 实验现象 | 结论 |
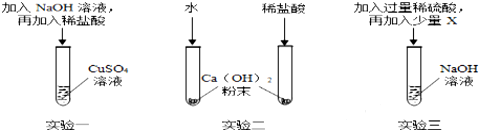
| 取少量上述反应后的溶液于试管中,滴加硫酸铜溶液 | 若生成蓝色沉淀 | 氢氧化钠溶液过量 |
| 若没有明显现象 | 稀盐酸与氢氧化钠溶液恰好完全反应 |
分析 酸溶液PH增大的原因可从物理或化学变化的角度分析,酸溶液被稀释其pH增大,酸中的氢离子被消耗其pH增大,氢氧化钠与盐酸反应生成氯化钠和水.
设计实验探究稀盐酸与氢氧化钠溶液的反应是否放热可以通过测定反应前后溶液的温度来进行确定,反应后的溶液中若氢氧化钠剩余,则加入硫酸铜会产生氢氧化铜蓝色沉淀,若无明显现象,则说明无氢氧化钠,剩余溶液可能为中性也可能为酸性.
解答 解:(1)酸溶液被稀释其pH会增大,所以强调只有测得的pH≥7才能证明反应发生是想说明已经无盐酸了,所以本题答案为:排除因氢氧化钠溶液的加入,稀释盐酸而引起pH变大(或只有pH≥7才能说明盐酸已经反应掉了);
(2)设计实验探究稀盐酸与氢氧化钠溶液的反应是否放热可以通过测定反应前后溶液的温度来进行确定,所以本题答案为:
| 实验步骤 | 实验现象 |
| 取一定量10%的氢氧化钠溶液于烧杯,插入温度计测温度,加入适量10%的盐酸,用玻璃棒搅拌,再测温度. | 温度计示数上升 |
| 实验步骤 | 实验现象 |
| 取一定量10%的氢氧化钠溶液于烧杯,插入温度计测温度,加入适量10%的盐酸,用玻璃棒搅拌,再测温度. | 温度计示数上升 |
| 实验步骤 | 实验现象 | 结论 |
| 取少受上述反应后的溶液子 试管中.滴加硫酸铜溶液. | 若 生成蓝色沉淀 | 氢氧化钠溶液过量 |
| 若没有明显现象 | 稀盐酸与氢氧化钠溶液恰好 完全反应 |
点评 本题考查了氢氧化钠和盐酸的中和反应,设计实验证明反应是否恰好完全进行以及反应过程中的能量问题,完成此题,可以依据课本已有的知识.所以要求同学们在平时的学习中要加强基础知识的储备,以便能够灵活应用.


科目:初中化学 来源: 题型:选择题
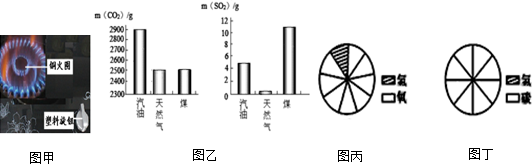
| A. | 实验记录:①用10mL量筒量取7.02mL水; ②用托盘天平称取5.6g氯化钠 | |
| B. | 安全常识:①酒精灯打翻起火,用湿抹布扑灭; ②冬天用煤炉取暖,应保证室内通风 | |
| C. | 化学与健康:①人体缺维生素A会引起夜盲症; ②禁止使用任何食品添加剂 | |
| D. | 化学与生活:①用钢丝球擦洗铝锅上的污垢; ②用食醋除水垢 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 服用含氢氧化铝的药物治疗胃酸过多 Al(OH)3+3HCl═AlCl3+H2O 复分解反应 | |
| B. | 拉瓦锡研究空气成分 2Hg0$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+02↑ 分解反应 | |
| C. | 用天然气作燃料 CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 氧化反应 | |
| D. | 验证铜和铝的活动性 Cu+AlS04═CuS04+Al 置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
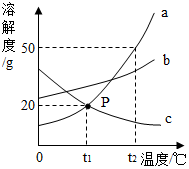 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
| 反应前 | 反应后 |  | ||
| A | B | C | D | |
 | 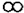 |  |  | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com