


分析 (1)根据制取玻璃的原理写出反应的化学方程式;
(2)①根据溶质质量分数的计算公式分析判断;
②N根据aHCO3受热分解的反应写出反应的化学方程式,根据反应的特点分析反应类型;
③根据整个生产过程分析循环利用的物质.
(3)①根据鸡蛋壳的主要成分是碳酸钙,与酸反应后蛋壳残渣质量为4.3g,因碳酸钙能与酸反应,则可计算碳酸钙的质量;
②根据质量守恒定律可以求出二氧化碳的质量;
③根据二氧化碳的质量结合反应的化学方程式可以计算出盐酸中溶质的质量,然后求出稀盐酸中溶质的质量分数即可
解答 解:(1)由制取玻璃的原理可知,在高温条件下石英砂(SiO2)与碳酸钠两种固体混合,生成硅酸钠(Na2SiO3)与二氧化碳,该反应的化学方程式为Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑;
故答为:(1)Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑;
(2)①精盐水经过蒸发浓缩转化为饱和食盐水的过程中,溶液中溶质的质量分数将变大;
②NaHCO3受热分解的化学反应方程式可以表示为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,该反应由一种物质生成了三种物质,属于基本反应类型中的分解反应;
③由整个生产过程可知,可循环利用的物质为:CO2和NH3.
答案:①变大;②2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;分解;③CO2和NH3.
(3)因碳酸钙与酸反应,杂质成分既不溶于水也不与酸反应,所以碳酸钙的质量为10g-2.5g=7.5g,
根据质量守恒可知CO2的质量为:10g+100g-106.7g=3.3g,
设所用盐酸中溶质的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
73 44
x 3.3g
$\frac{73}{x}=\frac{44}{3.3g}$
解得:x≈5.48g
所用盐酸的溶质质量分数是:$\frac{5.48g}{100g}$×100%=5.48%
答:所用盐酸的溶质质量分数是5.48%.
故答案为:7.5g;
3.3g;
所用盐酸的溶质质量分数是5.48%.
点评 本题考查了学生对物质的性质和流程图的分析,注重对学生解读解能力的考查,有利于培养学生的探究能力.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | 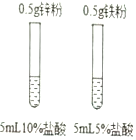 比较Zn和Fe的金属活动性强弱 比较Zn和Fe的金属活动性强弱 | B. | 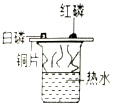 探究燃烧是否需要氧气 探究燃烧是否需要氧气 | ||
| C. | 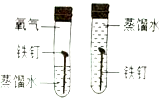 探究铁钉生锈时O2是否参与反应 探究铁钉生锈时O2是否参与反应 | D. |  测定空气中O2的含量 测定空气中O2的含量 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
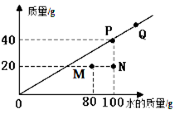 t℃测得某物质(不含结晶水)在不同质量的水中溶解达到饱和状态时所溶解该物质的质量,绘制成如图中斜线.下列说法错误的是( )
t℃测得某物质(不含结晶水)在不同质量的水中溶解达到饱和状态时所溶解该物质的质量,绘制成如图中斜线.下列说法错误的是( )| A. | t℃时该物质的溶解度为40g | |
| B. | N点表示溶液中溶质的质量分数为20% | |
| C. | 加溶质能使M点的溶液达到饱和状态 | |
| D. | 图中4点表示的溶液中溶质质量分数的关系是:N<M<P=Q |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
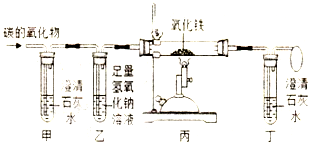
| A. | 若甲试管内溶液无变化,丁试管内石灰水变浑浊,则该碳的氧化物成分为一氧化碳 | |
| B. | 丙装置玻璃管中若发生化学反应,则一定为置换反应 | |
| C. | 若甲试管内溶液变浑浊,丁试管内无明显现象,则该碳的氧化物成分为二氧化碳 | |
| D. | 若甲试管和丁试管内溶液都变浑浊,丙处玻璃管内的红色固体变成黑色,则该碳的氧化物成分为一氧化碳和二氧化碳的混合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 能源是国家和家庭中必不可少的.
能源是国家和家庭中必不可少的.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com