
 构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的化学性质知识网络,如图所示,请结合图示回答下列问题:
构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的化学性质知识网络,如图所示,请结合图示回答下列问题:分析 (1)如用湿润的pH试纸测定盐酸的pH,相当于稀释了待测液,溶液的酸性变弱,当溶液的pH小于7时,呈酸性,且pH越小,酸性越强,据此进行分析解答.
(2)图中③是盐与盐酸反应生成新盐和新酸,据此结合盐酸的化学性质,进行分析解答.
(3)图中性质④是酸和碱反应生成盐和水,据此进行分析解答.
解答 解:(1)如用湿润的pH试纸测定盐酸的pH,相当于稀释了待测液,溶液的酸性变弱,当溶液的pH小于7时,呈酸性,且pH越小,酸性越强,则测得的pH结果比实际值偏大.
(2)图中③是盐与盐酸反应生成新盐和新酸,盐酸能与硝酸银溶液反应生成氯化银白色沉淀和硝酸,反应的化学方程式为:HCl+AgNO3═HNO3+AgCl↓.
(3)图中性质④是酸和碱反应生成盐和水,是盐酸与碱反应生成盐和水,是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应.
故答案为:(1)偏大;(2)HCl+AgNO3═HNO3+AgCl↓;(3)复分解.
点评 本题难度不大,掌握酸的化学性质(能与酸碱指示剂、活泼金属、金属氧化物、碱、一些盐等反应)并能灵活运用是正确解答本题的关键.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 A~F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示,已知A、B、C、D、E是不同类别的物质,C俗称纯碱,F是人体中含量最多的物质.(“→”表示转化关系,“-”表示反应关系;部分反应物、生成物及反应条
A~F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示,已知A、B、C、D、E是不同类别的物质,C俗称纯碱,F是人体中含量最多的物质.(“→”表示转化关系,“-”表示反应关系;部分反应物、生成物及反应条查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | BaCl2+Mg(NO3)2═Ba(NO3)2↓+MgCl2 | B. | Na2SO4+BaCO3═BaSO4↓+Na2CO3 | ||
| C. | H2SO4+NaOH═Na2SO4+H2O | D. | CO2+2KOH═K2CO3+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
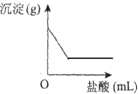 有一包白色固体,可能含有CaCO3、Na2SO4、NaOH、BaCl2中的一种或几种.取样溶于水,有沉淀产生;过滤后向沉淀中滴加盐酸有气体产生,沉淀的量与加入盐酸体积的关系如图所示.由此推断白色固体中( )
有一包白色固体,可能含有CaCO3、Na2SO4、NaOH、BaCl2中的一种或几种.取样溶于水,有沉淀产生;过滤后向沉淀中滴加盐酸有气体产生,沉淀的量与加入盐酸体积的关系如图所示.由此推断白色固体中( )| A. | 沉淀只有CaCO3 | |
| B. | 沉淀物一定有BaSO4和CaCO3 | |
| C. | 溶液中可能有CaCO3和NaOH,一定有Na2SO4,BaCl2 | |
| D. | 溶液中一定有Na2SO4,BaCl2和CaCO3,一定没有NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |


查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com