
| A. | ②③④⑤ | B. | ①③⑤ | C. | ①③④⑤ | D. | ①②③⑤ |
分析 根据质量守恒定律,化学反应前后元素的质量不变进行解答.
解答 解:8.8g CO2和3.6g H2O中含有碳元素和氢元素的质量分别为:8.8g×$\frac{12}{44}$×100%=2.4g,3.6g×$\frac{1×2}{18}$=0.4g,根据质量守恒定律,二氧化碳中的碳和水中的氢全部来自物质R,2.4g+0.4g=2.8g,故物质R中只含有碳、氢两种元素;并且碳、氢元素的质量比为:2.4g:0.4g=6:1,设R的化学式为CxHy,则12x:y=6:1,则x:y=1:2,综合以上分析可知①③⑤正确.
故选B
点评 本题考查了质量守恒定律以及根据化学式的计算,题目教有难度.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
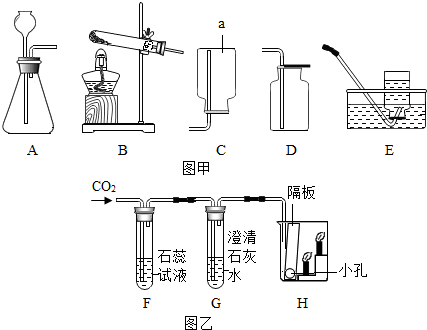
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
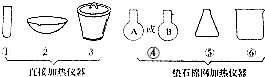
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Mg和MgCO3 | B. | CaO和CaCO3 | C. | CaO和Ca(OH)2 | D. | Mg和MgO |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
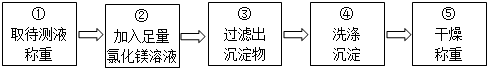
 某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下探究.
某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下探究.| 实验步骤 | 实验现象 | 实验结论 |
| 取样,滴加几滴无色酚酞试液 | 溶液变红色 | 待测液中含有氢氧化钠. |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁粉和硫酸铜溶液 | B. | 硝酸钡溶液和稀硫酸 | ||
| C. | 二氧化碳通入足量石灰水 | D. | 碳酸钠粉末和稀盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com