
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
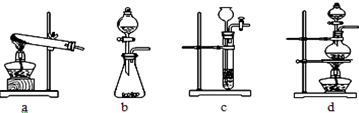
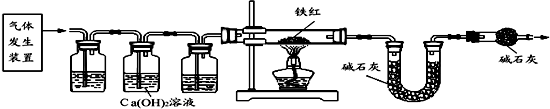
分析 草酸晶体(H2C2O4•3H2O)在浓硫酸作用下受热分解,因此选用d装置;实验前应先检查装置的气密性,二氧化碳一般用氢氧化钠溶液吸收,用澄清的石灰水检验,还可以检验二氧化碳是否除尽,二氧化碳可以用浓硫酸干燥;加热之前通入一氧化碳的目的是:将装置中的空气排出,防止发生爆炸;加热之后通入一氧化碳的目的是:驱赶装置中滞留的二氧化碳,使其全部被E装置中碱石灰全部吸收.一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,配平即可;如果全部是氧化铁,铁的最少量是10g×70%=7.0g,如果全部是氧化亚铁,铁的最大量是10g×77.8%=7.78g;E装置增重6.6g,那么二氧化碳是6.6g,氧元素的质量=6.6g×$\frac{32}{44}$=4.8g,因为4.8g氧元素的质量一半来自于一氧化碳,一半来自于铁的氧化物,那么铁红中氧元素的质量是4.8g÷2=2.4g,则铁红中铁的质量分数=$\frac{10g-2.4g}{10g}$×100%=76.0%;本实验中如果缺少C装置,水蒸气会通过,E装置也具有吸水性,因此E装置会增重,氧元素的质量偏大,则测得样品中铁的质量分数会偏小;实验装置的一个明显缺陷:缺少尾气处理装置或检验水是否除尽.
解答 解:(1)草酸晶体(H2C2O4•3H2O)在浓硫酸作用下受热分解,因此选用d装置,故答案为:d
(2)实验前应先检查装置的气密性,故答案为:检查装置的气密性
(3)二氧化碳一般用氢氧化钠溶液吸收,用澄清的石灰水检验,还可以检验二氧化碳是否除尽,一氧化碳可以用浓硫酸干燥;故答案为:c;a
(4)A装置中氢氧化钠吸收二氧化碳,化学反应方程式为CO2+2NaOH=Na2CO3+H2O;
(5)B装置还可以检验二氧化碳是否除尽,故答案为:验证二氧化碳已除尽
(6)加热之前通入一氧化碳的目的是:将装置中的空气排出,防止发生爆炸;加热之后通入一氧化碳的目的是:驱赶装置中滞留的二氧化碳,使其全部被E装置中碱石灰全部吸收.故答案为:①将装置中的空气排出,防止发生爆炸;②驱赶装置中滞留的二氧化碳,使其全部被E装置中碱石灰全部吸收.(合理即可)
(7)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,配平即可;故答案为:3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,(一氧化碳与FeO、Fe3O4也可以)
(8)如果全部是氧化铁,铁的最少量是10g×70%=7.0g,如果全部是氧化亚铁,铁的最大量是10g×77.8%=7.78g;E装置增重6.6g,那么二氧化碳是6.6g,氧元素的质量=6.6g×$\frac{32}{44}$=4.8g,因为一个一氧化碳分子只能抢氧化铁中一个氧原子变成二氧化碳,因此氧元素的质量一半一半,4.8g氧元素的质量一半来自于一氧化碳,一半来自于铁的氧化物,那么铁红中氧元素的质量是4.8g÷2=2.4g,则铁红中铁的质量分数=$\frac{10g-2.4g}{10g}$×100%=76.0%;故答案为:①7.0;7.78;②76.0%
实验反思:本实验中如果缺少C装置,水蒸气会通过,E装置也具有吸水性,因此E装置会增重,氧元素的质量偏大,则测得样品中铁的质量分数会偏小;实验装置的一个明显缺陷:缺少尾气处理装置.故答案为:偏小;缺少尾气处理装置.
点评 本考点属于实验探究题,实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验现象和分析,得到了正确的结论,属于实验过程和结论的探究.同学们要具体分析,综合掌握.本题型主要出现在实验题中.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 细铁丝在氧气中燃烧:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | |
| B. | 铁丝与硫酸铜溶液反应:Fe+CuSO4═Cu+FeSO4 | |
| C. | 碳不完全燃烧:2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO | |
| D. | 用赤铁矿石(主要成分:Fe2O3)炼铁:CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 图中单质的化学式为N2 | B. | 反应前后原子个数不变 | ||
| C. | 反应物都属于氧化物 | D. | 反应前后分子个数不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com