
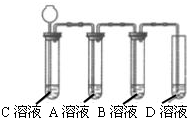
氯化氢气体溶于水得到盐酸.如图所示,将气体X和气体Y同时通入液体Z中,最终一定能看到液体变浑浊的是
| 序号 | 气体X | 气体Y | 液态Z |
| A | H2 | N2 | 水 |
| B | HCl | CO2 | 石灰水 |
| C | CO2 | O2 | 氯化钙溶液 |
| D | CO2 | CO | 足量石灰水 |

科目:初中化学 来源: 题型:阅读理解
 实验盒中有7种没有标签的溶液,老师让化学实验小组同学鉴别这些溶液.
实验盒中有7种没有标签的溶液,老师让化学实验小组同学鉴别这些溶液.| 溶液 | A | B | C | D |
| 加入盐酸后的现象 | 无明显现象 | 无明显变化 | 有气泡产生 | 无明显变化 |
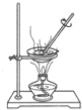
| 实验步骤 | 实验现象和结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| 密度(ρ)/g?ml-1 | 1.00 | 1.02 | 1.04 | 1.06 | 1.08 | 1.10 | 1.12 | 1.14 | 1.16 | 1.185 |
| 溶质质量分数(w)/% | 0.4 | 4.4 | 8.5 | 12.5 | 16.5 | 20.4 | 24.2 | 28.2 | 32.2 | 37.2 |
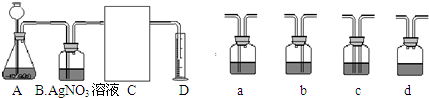
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com