
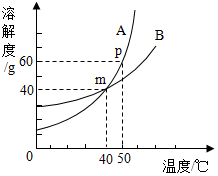
 小明同学绘制了如图所示A、B两种固体物质的溶液度曲线:
小明同学绘制了如图所示A、B两种固体物质的溶液度曲线:分析 (1)曲线的交点表示两物质的溶解度此时相等;
(2)根据50℃时,乙物质的溶解度进行分析解答;
(3)根据溶解度受影响的大小,选择结晶的操作方法--蒸发结晶或冷却结晶.溶解度受温度影响不大的物质结晶时一般采取蒸发结晶的方法,溶解度受温度影响较大的物质结晶时一般采取冷却结晶的方法;
(4)通过生活现象分析纯碱的溶解性特征,在曲线中找出对应的曲线;
解答 解:(1)从图中可以看出A和B的交叉点m,处在温度为40℃,溶解度为40g的交叉点上.也就是说m点时AB的溶解度相同.所以m点的含义是:在40℃时,A与B物质溶解度相等,均为40g.故填:40;
(2)根据图示可以看出,50℃时,乙物质的溶解度为60g,故溶质质量分数为:$\frac{60g}{100g+60g}×100%=37.5%$,故填:60g;37.5%;
(3)从图中可以看出B的溶解度受温度的影响不大,可以用蒸发结晶的方法析出结晶.故填:加热蒸发;
(4)夏天晒盐是因为食盐的溶解度受温度变化的影响不大,通过水分蒸发而获得食盐晶体.那么“冬天捞碱”则可以说明纯碱是利用冬季气温降低析出纯碱晶体,即冷却结晶,这说明纯碱的溶解度受温度变化的影响较大,这与曲线A较为一致.故填:A.
点评 本题主要考查了对固体溶解度的概念的理解和固体溶解度曲线的意义,以此培养学生的理解能力、培养学生分析问题、解决问题的能力.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:初中化学 来源: 题型:选择题
| A.除杂的方法 | B.化学物质中的“三” |
| 除去CO中的CO2--通过NaOH溶液 木炭粉中混有铁粉--用磁铁吸引 除去空气中的氧气--通过灼热的铜粉 | 三大化石燃料--煤、天然气、石油 三种黑色氧化物--CuO、MnO2、Fe3O4 稀释溶液三个步骤--计算、量取、混匀 |
| C.日常物质的区别 | D.实验安全注意事项 |
| 硬水和软水--加肥皂水并搅拌 酱油和食醋--闻气味 铁片和钢片--相互刻划,比较硬度 | 制取气体--先检查装置的气密性 厨房天然气泄漏--要立即打开换气扇 油锅着火--用水烧灭 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用铝合金制飞机外壳是因其硬度大、密度小、耐腐蚀 | |
| B. | 发射火箭采用的液氢、液氧都是无污染的纯净物 | |
| C. | 稀有气体通电时会发出各种颜色的光,利用的是其学性质稳定 | |
| D. | 生活中常用加热煮沸的方法降低水的硬度 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 实验目的 | 试剂或方法 |
| A | 鉴别FeCl3、NaCl、NaOH、MgCl2四种溶液 | 不另加试剂 |
| B | 鉴别CaCO3、NaCl、NaOH、NH4NO3四种固体粉末 | 水 |
| C | Na2SO4溶液与AgNO3溶液 | 分别加入BaCl2溶液 |
| D | 除去氮气中的少量氧气 | 通过灼热的铜网 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com