
| A. | 硫和氧 | B. | 氢和氧 | C. | 只有硫 | D. | 氢、硫、氧 |
分析 根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,结合各化学式进行解答本题.
解答 解:氢元素显+1价,设H2S中硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x=0,则x=-2价.
氧元素显-2价,设SO2中硫元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:y+(-2)×2=0,则y=+4价.
硫元素的化合价由-2价变为+4价.
根据单质中元素的化合价为0,O2属于单质,故氧元素的化合价为0;生成物二氧化硫、水中氧元素显-2价.氧元素的化合价由0变为-2价.
故在反应前后,化合价发生了变化的元素S、O.
故选A.
点评 本题难度不大,掌握利用化合价的原则(单质中元素的化合价为0、在化合物中正负化合价代数和为零)计算指定元素的化合价的方法即可正确解答本题.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
| 主要物质(杂质) | 化学方程式(或方法) |
| FeSO4(CuSO4) | |
| KCl(K2CO3) | |
| KCl(K2SO4) | |
| CO2(CO) | |
| CO(CO2) | |
| NaNO3(CuSO4) | |
| KNO3(NaCl) |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 风助火威--为燃烧提供足够多的氧气 | |
| B. | 杯水车薪一水少了不能降低温度使温度低于可燃物的着火点 | |
| C. | 釜底袖薪一隔离可燃物可以灭火 | |
| D. | 水火不容--用水可以灭火,是因为降低了可燃物的着火点 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 我们学习过常见气体的实验室制法,知道了制取气体的一般思路和方法.
我们学习过常见气体的实验室制法,知道了制取气体的一般思路和方法.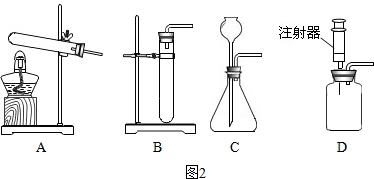
| 盐酸 | 大理石 | 温度条件 |
| 5% | 细颗粒 | 20℃ |
| 10% | 粗颗粒 | 40℃ |
| 每次用量均20mL | 每次用量均5g |
| 实验编号 | 温度 | 大理石规格 | HCl浓度 | 探究目的 |
| ① | 20℃ | 粗颗粒 | 5% | (I)实验①和②探究浓度对反应快慢的影响; (II)实验②和④探究温度对反应快慢的影响; (III)实验①和③③探究大理石粗、细对反应快慢的影响. |
| ② | 20℃ | 粗颗粒 | 10% | |
| ③ | 20℃ | 细颗粒 | 5% | |
| ④ | 40℃ | 粗颗粒 | 10% |
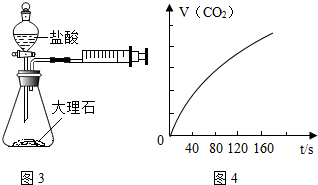 实验探究时,他们每次收集CO2气体均为40mL,则实验中他们还应记录的实验数据是收集40mL的CO2所需要的时间.图4是根据某次实验数据作出的CO2和时间变化的关系曲线,请分析在80秒以后,产生CO2逐渐减慢的可能原因:80秒后,盐酸反应了一部分,盐酸的浓度变低,反应速率变慢.
实验探究时,他们每次收集CO2气体均为40mL,则实验中他们还应记录的实验数据是收集40mL的CO2所需要的时间.图4是根据某次实验数据作出的CO2和时间变化的关系曲线,请分析在80秒以后,产生CO2逐渐减慢的可能原因:80秒后,盐酸反应了一部分,盐酸的浓度变低,反应速率变慢.查看答案和解析>>
科目:初中化学 来源: 题型:填空题

| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀硫酸过量 |
| 方案二 | 取样,滴入几滴紫色石蕊试液 | 溶液变红 | 稀硫酸过量 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 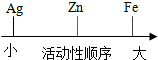 部分金属活动性顺序 | B. | 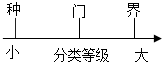 生物的分类等级 | ||
| C. | 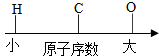 部分元素的原子序数 | D. | 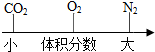 空气中部分成分的体积分数 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁在潮湿的空气中容易生锈 | B. | 大理石、金刚石都是无机材料 | ||
| C. | 铝合金比铝的强度和硬度高 | D. | 合金、合成纤维都是有机合成材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com