
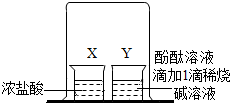
 根据如图实验,判断下列说法错误的是( )
根据如图实验,判断下列说法错误的是( )| A. | 浓盐酸有挥发性 | B. | HCl分子在不断运动 | ||
| C. | Y杯溶液颜色会改变 | D. | Y杯内发生了置换反应 |
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 | |
| 小东 | 用玻璃棒蘸取溶液滴到pH试纸上,对照比色卡并读出pH | pH试纸变色 pH>7(填“>”或“<”) | 该溶液是氢氧化钠溶液 |
| 小南 | 取适量溶液于试管中,加入经打磨过的铝条 | 有气泡产生 | 该溶液是稀硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 气凝胶常温下氧化学性质很不稳定 | |
| B. | 气凝胶具有很强的吸附作用 | |
| C. | 气凝胶是一种化合物 | |
| D. | 气凝胶在氧气中完全燃烧的产物是CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫在氧气中燃烧,发出淡蓝色火焰,说明硫具有可燃性 | |
| B. | CO2通入石蕊溶液中,紫色溶液变红色,说明CO2显酸性 | |
| C. | 某物质加碱研磨,闻到刺激性氨味,说明物质中含有铵根 | |
| D. | 锈钉放入盐酸中,无色溶液变黄色,说明盐酸能与铁反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
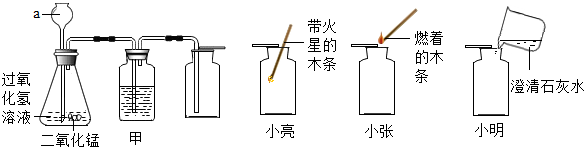
 利用如图所示的仪器和药品,测量一定质量大颗粒食盐晶体的体积,同学们展开了讨论.(不考虑杂质对实验的影响)
利用如图所示的仪器和药品,测量一定质量大颗粒食盐晶体的体积,同学们展开了讨论.(不考虑杂质对实验的影响)查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
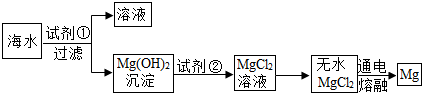
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com