

 ×100%=88.3%
×100%=88.3% 

科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2009年黑龙江省大庆市中考化学试题 题型:058
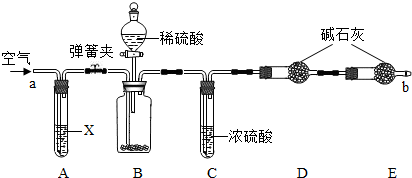
侯氏制碱法所得的纯碱中常含有少量氯化钠,现用下图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等固定装置已略去).
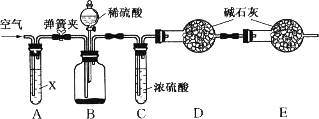
实验步骤如下:
①按图连接装置,并检查气密性;
②准确称得盛有碱石灰(固体氢氧化钠和氧化钙的混合物)的干燥管D的质量为83.4 g;
③准确称得6.0 g纯碱样品放入装置B的广口瓶中;
④打开装置B的分液漏斗旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为85.6 g.
试回答:
(1)鼓入空气的目的是________,装置A中试剂X最适宜选用________.
(2)若没有C装置,则会导致测定结果________(填:“偏大”或“偏小”).
(3)E装置的作用是________.
(4)请根据实验中测得的有关数据,计算纯碱样品中碳酸钠的质量分数.(要求:写出计算过程,结果保留1位小数)
查看答案和解析>>
科目:初中化学 来源:2012年初中毕业升学考试(黑龙江哈尔滨卷)化学(带解析) 题型:计算题
侯氏制碱法为纯碱工业的发展做出了杰出的贡献.用此方法制得的工业纯碱产品中会含有一定量的氯化钠.为测定一种用侯氏制碱法生产的工业纯碱产品中碳酸钠的纯度,现取26.5g该工业纯碱样品.加入100g某溶质质量分数的稀盐酸,恰好完全反应,得到117.7g不饱和溶液.请回答下列问题:
(1)加入稀盐酸发生反应的化学方程式为 ;
(2)求解样品中碳酸钠质量(x)的比例式为 ;
(3)样品中碳酸钠的纯度为 ;
(4)若向反应后的溶液中加入54.5g水,则所得溶液中溶质和溶剂的质量最简比为 ;
(5)工业上常用碳酸钠和氢氧化钙反应来制取氢氧化钠.若要用这种方法制得20t含氢氧化钠80%的工业烧碱,需要上述用侯氏制碱法获得的工业纯碱产品的质量是 .
查看答案和解析>>
科目:初中化学 来源:2012年初中毕业升学考试(黑龙江哈尔滨卷)化学(解析版) 题型:计算题
侯氏制碱法为纯碱工业的发展做出了杰出的贡献.用此方法制得的工业纯碱产品中会含有一定量的氯化钠.为测定一种用侯氏制碱法生产的工业纯碱产品中碳酸钠的纯度,现取26.5g该工业纯碱样品.加入100g某溶质质量分数的稀盐酸,恰好完全反应,得到117.7g不饱和溶液.请回答下列问题:
(1)加入稀盐酸发生反应的化学方程式为 ;
(2)求解样品中碳酸钠质量(x)的比例式为 ;
(3)样品中碳酸钠的纯度为 ;
(4)若向反应后的溶液中加入54.5g水,则所得溶液中溶质和溶剂的质量最简比为 ;
(5)工业上常用碳酸钠和氢氧化钙反应来制取氢氧化钠.若要用这种方法制得20t含氢氧化钠80%的工业烧碱,需要上述用侯氏制碱法获得的工业纯碱产品的质量是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com