
 43、在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:
43、在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验: 验的基础上,设计一个补充实验来实现探究目的.他两若按如图所示的实验探究时,你决定推荐:
验的基础上,设计一个补充实验来实现探究目的.他两若按如图所示的实验探究时,你决定推荐:

科目:初中化学 来源: 题型:
 29、我们的日常生活离不开金属.
29、我们的日常生活离不开金属.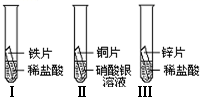
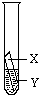 ①一段时间后,可观察到实验Ⅱ的现象是
①一段时间后,可观察到实验Ⅱ的现象是查看答案和解析>>
科目:初中化学 来源: 题型:
 在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)
在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
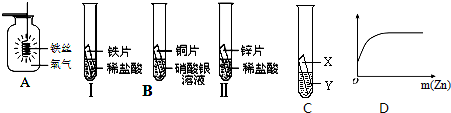
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com