
(7分)人类的生产生活离不开金属。
(1)铁生锈的条件是铁与 直接接触。
(2)铜制品如果长期暴露在空气中也会生锈,已知铜锈化学式为Cu2(OH)2CO3。试判断铜生锈除满足铁生锈的上述条件外,还需要空气中的__________。
(3)在生活中经常用一些铝制品代替铁,铝耐腐蚀的原因是___________。[填序号]
A. 铁比铝活动性弱
B. 铝与氧气反应在其表面生成致密的氧化物保护膜
C. 常温下,铝不与稀盐酸、稀硫酸等稀酸溶液反应
(4)如右图所示,烧杯中盛有质量相等、质量分数相等的稀盐酸,天平调平后,同时向其中分别加入等质量的锌片和铁片,则从反应开始到金属完全反应的过程中,天平指针指向的变化是 。[填序号]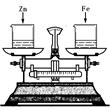
A.向左偏 B.向右偏
C.先向左偏后向右偏 D.先向右偏后向左
(5)向一定量的铁粉中逐滴加入稀硫酸至过量,右图是反应过程中某种物质的质量Y随加入稀硫酸的质量变化的关系,则Y可能表示 。[填序号]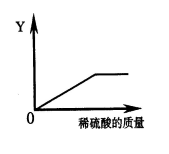
A.消耗铁粉的质量 B.生成硫酸亚铁的质量
C.溶液的总质量 D.生成氢气的质量
(1)水和氧气 (2)二氧化碳(3)B (4)D (5)BD
解析试题分析:(1)钢铁在潮湿的空气中最容易生锈,说明铁生锈的条件是水与氧气。
(2)由Cu2(OH)2CO3化学式可以看出铜锈的成分中含有碳元素,根据质量守恒定律,化学变化过程中元素的种类不变可知,铜生锈还需要空气中的二氧化碳参与反应。
(3)铝的活动性比铁强,在空气中,铝易与空气中的氧气反应,生成一层致密的氧化铝保护膜,隔绝了铝与氧气的进一步接触,从而阻止了铝的进一步反应,故选B。
(4)加入锌与铁后,由于锌的活动性比铁强,反应速度较快,质量减轻较快,故指针先向右偏;而最后是由于铁生成的氢气的质量较多,即减轻的多,所以锌的一边质量较大,因此指针又偏向左,故选D。
(5)铁和硫酸反应生成硫酸亚铁和氢气,由于铁是定量的反应物,故铁的质量会越来越小,直至为0;硫酸亚铁和氢气是生成物,故随反应的进行,质量会由0开始不断增大,直到铁完全反应,质量就不再改变;由图可知,图象中表示的物质Y的量是随硫酸量的增加而增加,达到一定高度时不再增加(此时铁已完全反应),符合氢气和硫酸亚铁的质量变化趋势;而C溶液的总质量,会硫酸的加入一直增加,故选BD。
考点:金属的化学性质,常见金属的特性及其应用,金属活动性顺序及其应用,金属锈蚀的条件及其防护,根据化学反应方程式的计算
点评:本题围绕金属考查了多个知识点,其中天平问题和图象分析问题是重点,也是难点,解题的关键在于熟练掌握金属的性质,并要具有一定的识图能力和分析问题的能力。


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:初中化学 来源: 题型:
| W | X | Y | Z | |
| 稀盐酸 | × | √ | × | √ |
| Z(NO3)2溶液 | × | √ | × | |
| YNO3溶液 | √ | √ |
查看答案和解析>>
科目:初中化学 来源: 题型:

| 金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
| 熔点/℃ | 1083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 人类的生产生活离不开金属.(1)在地壳里含量居第二位的金属元素是
人类的生产生活离不开金属.(1)在地壳里含量居第二位的金属元素是查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
 人类的生产生活离不开金属,下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝.
人类的生产生活离不开金属,下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com