
 为了测定某种性质像钠的金属的相对原子质量,设计的装置如右图,该装置(包括水)的总质量为ag,将质量为bg的(不足量)此金属放入水中,应立即塞紧瓶塞,完全反应后,再称量该装置的总质量为cg.则:
为了测定某种性质像钠的金属的相对原子质量,设计的装置如右图,该装置(包括水)的总质量为ag,将质量为bg的(不足量)此金属放入水中,应立即塞紧瓶塞,完全反应后,再称量该装置的总质量为cg.则: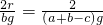

 ;
; 的计算结果产生气体质量(a+b-c)偏大而计算结果偏小;
的计算结果产生气体质量(a+b-c)偏大而计算结果偏小;

科目:初中化学 来源: 题型:
 为了测定某种性质像钠的金属的相对原子质量,设计的装置如右图,该装置(包括水)的总质量为ag,将质量为bg的(不足量)此金属放入水中,应立即塞紧瓶塞,完全反应后,再称量该装置的总质量为cg.则:
为了测定某种性质像钠的金属的相对原子质量,设计的装置如右图,该装置(包括水)的总质量为ag,将质量为bg的(不足量)此金属放入水中,应立即塞紧瓶塞,完全反应后,再称量该装置的总质量为cg.则:查看答案和解析>>
科目:初中化学 来源:2008年江苏省扬州市仪征市金升外国语实验学校中考化学模拟试卷(三)(解析版) 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com